人體的防禦
鋅離子運輸蛋白調控B淋巴細胞初期發育
鋅離子運輸蛋白調控B淋巴細胞初期發育(Zinc transporter regulates early B-cell development)
國立臺灣大學生命科學系范姜文榮編譯/國立臺灣師範大學生命科學系李冠群副教授責任編輯
編譯來源:亜鉛はB細胞の生存・維持に重要
鋅離子是生物體代謝的必要微量元素,若代謝異常,會引發糖尿病、味覺異常、皮膚病變、生殖機能下降、及免疫不全等。目前認為細胞內鋅離子濃度,受到鋅離子運輸蛋白(transporter)的調控。存在細胞內的鋅離子,擔任訊息傳遞的角色,在細胞內訊息傳遞控制扮演重要的角色。
觀察鋅離子運輸蛋白「ZIP13」基因缺失(gene deletion)大鼠,會出現骨骼、牙齒、皮膚等硬組織或結締組織的異常,目前已知ZIP13在骨骼形成相關的增殖因子BMP、或於組織發育、細胞分化等扮演重要角色的增殖因子TGF-β之訊息傳遞調控有關。另外,「ZIP14」基因缺失老鼠,會出現軟骨骨化、以及成長賀爾蒙生成、醣類生成等異常,因此瞭解ZIP14與賀爾蒙等訊息傳遞至細胞內G蛋白偶聯受體1的調控有關。
探索腸道免疫細胞與細菌間共生關係分子機制
探索腸道免疫細胞與細菌間共生關係分子機制(Exploring molecular mechanism between intestinal immune cells and gut microbiota)
國立臺灣大學生命科學系范姜文榮編譯/國立臺灣師範大學生命科學系李冠群副教授責任編輯
編譯來源:腸管免疫系と腸内細菌の共生関係の構築に必須の分子を発見
日本慶義義塾大學長谷教授領導的研究團隊,透過小鼠動物實驗,發現腸道免疫細胞與腸內細菌營造共生關係之關鍵分子-Uhrf1,Uhrf1能支持腸道調節性T細胞的增殖與運作,促使腸道T細胞防止對腸內細菌產生過度免疫反應,在維持大腸免疫系統恆定,扮演重要的角色。其研究成果2014年6月刊載於科學期刊「Nature Immunology」。
腸道免疫系統的特色,一方面需啟動免疫反應來排除病原性細菌等有害抗原;另一方面也有免疫耐受性(immune tolerance),以避免對食物性蛋白質或共生菌等無害抗原產生反應。目前認為免疫系統的反應失衡是造成食物過敏或腸道發炎的主要原因。
嗜鹼性白血球導致氣喘的機制
嗜鹼性白血球導致氣喘的機制(Asthma mechanism induced by basophils)
國立臺灣大學生命科學系范姜文榮編譯/國立臺灣師範大學生命科學系李冠群副教授責任編輯
編譯來源:白血球「好塩基球」の喘息における新メカニズムを解明
日本東京理科大學為主的研究團隊發現,居家塵螨等過敏原誘發的氣喘,由嗜鹼性白血球(basophil)分泌白介素-4(interleukin-4;IL-4)與自然輔助性細胞(natural helper cell)共同調控所形成。該研究成果2014年5月刊載於科學期刊「Immunity」。
人體具有防禦異物、保衛身體的免疫系統,但它有時會產生不適合的免疫反應,其一為「過敏反應」。過敏反應依形成機制可分為5大類別,其中免疫球蛋白E(immunoglobulin E; IgE)所引發的過敏反應I型,以支氣管氣喘、花粉症、及過敏性鼻炎為代表。針對特定過敏原(allergen),免疫球蛋白E會與肥大細胞(mast cell)或嗜鹼性白血球的受器結合,誘發過敏反應。
近年發現,即使在不存在免疫球蛋白E作用之肥大細胞或T淋巴球(T lymphocyte)的反應系,也會產生過敏反應。此類針對特殊抗原的免疫反應,可能與嗜鹼性白血球、或免疫系統之新型「自然淋巴球(natural lymphocyte)」有關聯,最近受到高度矚目。另外,蛋白質分解酵素-半胱氨酸蛋白酶(cysteine protease),如居家塵螨或鳳梨內所含有特殊酵素,是可以強烈誘導過敏反應的過敏原,當過度入侵氣管時,會破壞氣管上皮,釋放出白介素-33(IL-33)誘發過敏反應。
IL-33再與自然淋巴球之自然輔助性細胞產生作用,引發氣喘。嗜鹼性白血球占全體白血球比率不及0.5%,長久以來,其機能或生物特性仍然不清楚。東京理科大學的研究團隊為了解析嗜鹼性白血球在體內過敏反應所扮演的角色,特別製作嗜鹼性白血球缺損的基改小鼠(Bas-TRECK小鼠)、及僅嗜鹼性白血球IL-4缺損的基改小鼠。使用半胱氨酸蛋白酶,對小鼠予以點鼻處理,通常3天內,會導致嗜酸性白血球(eosinophil)大量聚集,造成肺部發炎,並導致黏蛋白(mucin)大量生成,顯現氣喘症狀。但Bas-TRECK小鼠,即使以半胱氨酸蛋白酶點鼻處理,也無氣喘症狀,且嗜酸性白血球聚集於肺部或黏蛋白生成,也都受到顯著抑制。在僅嗜鹼性白血球IL-4缺損的基改小鼠,氣喘症狀也同樣受到抑制。這些結果顯示嗜鹼性白血球所分泌IL-4,在氣喘發作扮演重要角色。
維他命A過量引發皮膚炎
維他命A過量引發皮膚炎(Excess Vitamin A induces dermatitis)
國立臺灣大學生命科學系范姜文榮編譯/國立臺灣師範大學生命科學系李冠群副教授責任編輯
編譯來源 : 過剰なビタミンAが引き起こす皮膚炎の原因を解明
日本東京大學醫學研究所等研究團隊,發現維生素A過量引發肥大細胞(mast cell)異常活化,誘發皮膚炎。該研究成果刊載於2014年4月17日免疫學科學期刊「Immunity」。
過去研究已知肥大細胞是引起過敏或發炎的一種免疫細胞,但在皮膚等之結締組織、以及肺或腸道等之黏膜組織的肥大細胞卻有不同的特性。肥大細胞在不同組織有不同特性的意義,以及其組織特異性的調節機制仍不明。
因此日本東京大學醫學研究所等研究團隊,首先比較存在於身體各種組織內的肥大細胞之基因表現差異,發現肥大細胞會因所在組織不同,而有不同的特性。接著並發現生物體內結締組織的纖維母細胞(fibroblast)與肥大細胞間,彼此積極進行交互作用,認為纖維母細胞可能具有調節肥大細胞組織特性的功能。再從身體各種組織,單離纖維母細胞及肥大細胞,一同置於試管中培養,發現肥大細胞能表現存在於各種組織下的特性。
研究團隊發現皮膚中肥大細胞的「P2X7受器」之基因表現比其他組織為少;且若將有「P2X7受器」基因表現之肥大細胞移植到小鼠皮膚內,數天後「P2X7受器」的基因表現量下降。研究團隊也發現皮膚內纖維母細胞之酵素Cyp26b1能代謝維他命A以調節其濃度,若此調節功能無法作用或皮膚出現過剩的維他命A,會引起肥大細胞過度活化,造成皮膚發炎;若小鼠未出現「P2X7受器」或肥大細胞,則不會引發皮膚發炎。肥大細胞「P2X7受器」能辨識因受傷或發炎而釋放至細胞外的ATP、或皮膚內豐富的抗菌肽,肥大細胞也會受到纖維母細胞調控改變特性,以應付皮膚的特殊環境。
DNA引發過敏反應
DNA引發過敏反應(Nucleic acid induces allergic inflammation)
國立臺灣大學生命科學系范姜文榮編譯/國立臺灣師範大學生命科學系李冠群副教授責任編輯
編譯來源 : アレルギー反応を引き起こす新たな誘導因子を発見
人體的免疫系統能分辨自身與外來物質的差異,並攻擊入侵的異物,如病原體,以保護身體免於傷害,此即為免疫反應。但是,有些異物並非病原體,對身體亦無危害,如花粉或室內灰塵等,一般人對這類異物不會產生明顯的免疫反應,過敏患者卻會被它們誘發過剩的免疫反應。
輔助性T細胞(Th)之一的「Th2」細胞,在免疫反應扮演重要角色。未曾與抗原接觸的初始T細胞 (naive T cell),會因接觸花粉等抗原後,分化為Th2細胞,誘發對特定抗原產生專一性過敏反應。初始T細胞,也能分化成輔助性T細胞(helper T cell)之一的「Th1」細胞。Th1細胞對去除入侵或寄生在細胞內的病原體,扮演重要的角色。
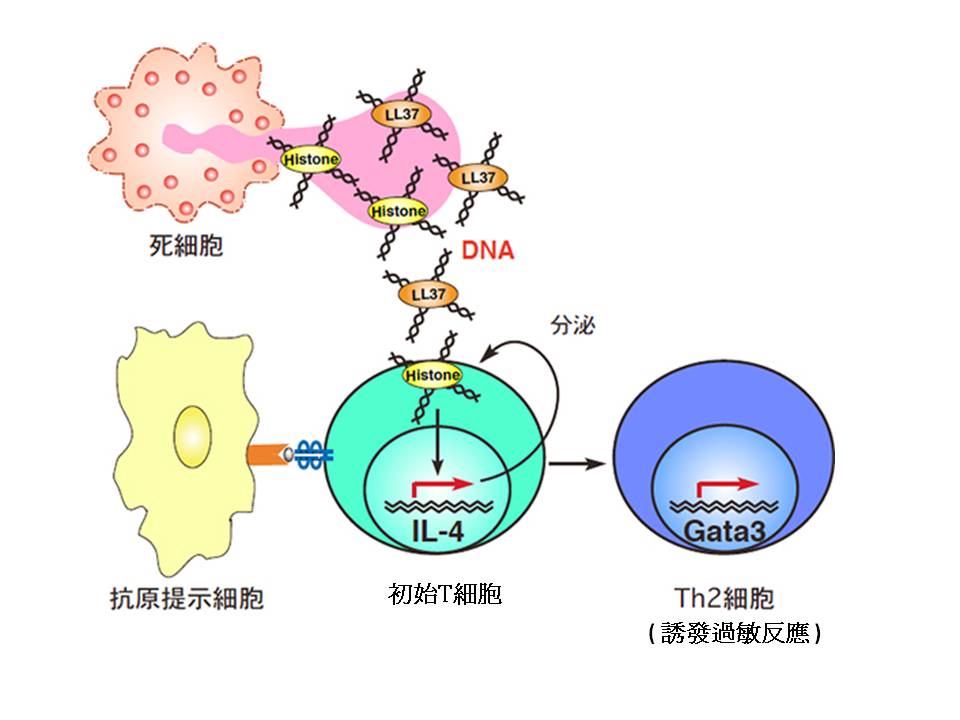
圖一 : 發炎反應導致死細胞產生,其所釋出DNA,會與組織蛋白(histone)、抗菌肽(LL37)形成複合體,進入初始T細胞,加上受到抗原提示細胞的刺激,初始T細胞分泌細胞介素IL-4,誘發分化為Th2細胞。
負責自然免疫的樹突細胞具有類鐸受體(Toll-like receptor),能接受病原體特有成分的刺激而被活化,在初始T細胞分化為Th1細胞的過程中扮演重要角色。但是,初始T細胞如何分化為Th2細胞的機制仍不明,日本理化學研究所的免疫訊息研究團隊因此嘗試解析其機制。研究團隊發現,死細胞釋出的DNA能誘導分化產生發炎性T細胞(inflammatory T cell),該研究成果刊載於2014年4月10日科學期刊「Nature Communications」線上版。
腸內細菌影響免疫力
腸內細菌影響免疫力
國立臺灣大學生命科學系助教范姜文榮
編譯來源:東京大學2013年7月11日學術發表《制御性T細胞を誘導するヒトの腸内細菌の同定と培養に成功 -炎症性腸疾患やアレルギー症に効果-》
日本東京大學新領域創成科學研究所附屬跨領域情報中心,與理化學研究所組成的共同研究團隊,首次成功辨識出人類腸內特定細菌群,能誘導調節性T細胞,具有抑制免疫反應及抗發炎功能。
過度免疫反應所導致的過敏或腸炎等病徵,其發病與T細胞有關。T細胞是屬於淋巴球的一種,具各式各樣已分化的T細胞型式,這些已分化的T細胞大致可分為「活化免疫T細胞」與「抑制免疫T細胞」,調節性T細胞是屬於抑制免疫機能的類別。免疫患者與自我免疫患者,有過度旺盛的自我免疫反應,其發病的主要原因,是由於調節性T細胞的數量太少,其抑制功能無法正常運作。因此如能以人為方式控制調節性T細胞的數量,就有希望協助治療各種免疫系統病患,減輕其症狀並且預防發病。
雖先前此研究團隊的本田博士等人,已於老鼠實驗中發現,在腸管內的調節性T細胞數量為其他臟器的3倍以上,並發現腸內細菌內,具有屬於格蘭氏陽性菌、能形成「芽孢」的梭狀桿菌屬細菌(Clostridium),需要調節性T細胞的誘導,但是經辨識出的腸內細菌均來自老鼠腸內。如要應用於人類疾病,有必要進行人體腸內細菌的辨識,再加上人體消化管內也存在許多梭狀芽孢桿菌屬細菌,有必要進一步研究能誘導調節性T細胞的人類腸內細菌。
本次研究將健康成人的糞便投與無菌老鼠,形成具有人體腸內細菌群聚的老鼠,此老鼠大腸內出現比無菌老鼠多的調節性T細胞,強烈顯示存在能誘導調節性T細胞機能的人體腸內細菌族群,經基因體全序列解析,發現此細菌族群是由梭狀芽孢桿菌屬的17種菌種所組成。
凝血機制(Coagulation)
凝血機制(Coagulation)
臺北市立第一女子高級中學二年級洪采媚
為什麼血會乾掉—凝血機制與其重要性
大家多少都有流過鼻血的經驗吧? 那麼你是否曾想過,若一直血流不止,會是多可怕的夢饜呢?
在我們在受傷之後,身體會啟動凝血機制,而凝血酶就像身體內的小護士,能幫助傷口止血癒合。
那到底什麼是凝血酶呢?
它是一種蛋白質水解酶,是凝血酶元藉凝血活酶和鈣離子的作用而成的纖維蛋白,能夠使溶在血漿中的纖維蛋白元(fibrinogen),轉變成不溶性的網狀結構,此結構就是我們耳熟能詳的纖維蛋白(fibrin)。纖維蛋白能固定血小板,形成血栓(thrombi)覆蓋在傷口,使血液產生凝結不再流出血管,維持血液流動的順暢。
如果血管堵塞會有什麼症狀呢?
有許多心血管疾病就是因為血栓阻塞血管,導致血液無法順暢流動,讓組織壞死、動脈栓塞,嚴重甚至還有致命的危險,可見在人體生理機能中,凝血酶扮演多麼重要的角色。
微生物與疾病(Microorganisms and Disease)
微生物與疾病(Microorganisms and Disease)
國立台灣師範大學生命科學研究所林汝黛碩士生/國立台灣師範大學生命科學系張永達副教授責任編輯
即使在微生物被發現後,人們仍不認為微生物與傳染疾病具有關連性。即使Edward Jenner能以接種牛痘來預防天花,但也無法解釋成功預防天花的原因。直至十九世紀的Casimir Davaine首度證明特殊微生物能引發特殊疾病。十九世紀末的Robert Koch已能將致病細菌分離,感染寄主後造成特定的感染症狀,證明了單一種細菌會引起單一種疾病。
在微生物與疾病的關係被建立後,微生物感染造成可傳染性疾病的這種概念,普遍的流傳。科學家在對煙草葉鑲嵌病的觀察與實驗後,認為引起這種疾病的原因也是細菌。但是因為它可以通過可濾出細菌的陶瓷濾網,當時的科學家推論病毒是一種與細菌類似的病原體,所不同的僅在於病毒必須在生活的細胞內才能繁殖,而且體積十分微小,能夠通過細菌濾器,也無法在光學顯微鏡下觀察。所以Martinus Willem Beijerinck在1898年另為這個史無前例的「小細菌」取名為Virus。
電子顯微鏡問世後,人類得以肉眼觀察病毒的形態。1939年,G.A.Kansche在電鏡下直接觀察到了菸草鑲嵌病毒(TMV)與番茄黃化花葉病毒(TYMV)的顆粒,並以奈米為單位指出了病毒的大小。1953年,科學家們注意到病毒的增殖必定需要有活體細胞的存在。