血青素(Hemocyanin)
血青素(Hemocyanin)
台北市立第一女子高級中學生物科許一懿老師/國立台灣大學動物學研究所陳俊宏教授責任編輯
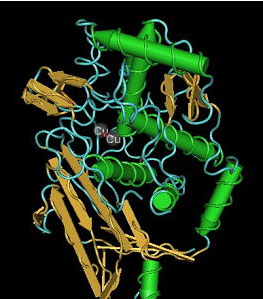
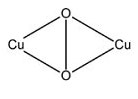
血青素又稱為血青蛋白,和血紅素類似,是一種與呼吸作用有關的含金屬蛋白質。血青素利用兩個亞銅離子(Cu+)與一個氧分子(O2)連結以攜帶氧氣,氧化作用會造成血青素顏色的改變。在未與氧分子結合時,Cu+顯現無色,但和氧結合後,Cu+氧化成Cu2+,血青素就會呈現藍色。
在動物體內,利用血紅素來攜帶氧氣的方式是最常見的,其次則是血青素。大多數的軟體動物與部分的節肢動物,包括被視為活化石的鱟(Limulus polymephus),都是以血青素來輸送氧氣。雖然這兩者的功能相似,但是它們的分子構造和作用機制卻是大不同:血紅素的金屬離子鐵是和血基質(heme)結合,血青素的銅則是和組織胺酸(Histidine)形成輔基;血紅素常位於紅血球內,血青素卻是懸浮於血淋巴中;血紅素的分子較小,血青素則因生物種類不同而由2個或6個次單位構成二聚體(Dimer)或是六聚體(Hexamer),每個次單位都有氧分子的結合部位,大小約為75kDa,這些二聚體或六聚體還可以進一步連結,排列成鏈狀或是團狀,整體的分子量可超過1500kDa。由於血青素的分子量大,可以游離在血淋巴中,增強其攜帶的氧量,不過,這種游離的血青素會增加血液的黏稠度,造成血液循環的過程需消耗較多的能量。相反的,由於血紅素分子量小,若游離在血液或淋巴中,會造像腎臟等過濾器官的工作負擔,因此大多被包覆於紅血球內。
一般而言,相同體積的血液中,血青素攜帶氧氣的效率不若血紅素好,大約僅達1/4。然而在部分甲殼類動物體內,血青素和氧分子結合後,進一步再與氧氣的結合率會提高,也就是具有協同鍵結(cooperative binding)的效果,因此希爾係數(Hill coefficient)可高達1.6~3.0,非常接近血紅素的希爾係數數值2.8~3.0。在這些動物體內,血青素由六個次單位構成六聚體,只要有一個次單位和氧分子結合後,鄰近次單位對氧氣的親和力都會跟著提高,由於這些六聚體和其他六聚體形成聚合物,整個大分子對氧分子的親和力都變得更高。
近年來,科學家發現智利鮑魚(Concholepas concholepas)的血青素對於膀胱癌和攝護腺癌具有免疫療效。在一項2006年的老鼠實驗中發現,以此血青素處理過的老鼠,在植入膀胱腫瘤細胞(MBT-2)後,具有明顯的抗癌效果,不僅存活率較高,腫瘤細胞的生長也受到明顯的控制,此結果提供進一步應用的可能性。
參考資料:
Hemocyanin. http://en.wikipedia.org/wiki/Hemocyanin


 前一篇文章
前一篇文章 下一篇文章
下一篇文章 戀愛活化大腦多巴胺神經
戀愛活化大腦多巴胺神經 ![[新聞] 發現臺灣目前最古老人類化石](https://highscope.ch.ntu.edu.tw/wordpress/wp-content/uploads/2015/01/pe.png) [新聞] 發現臺灣目前最古老人類化石
[新聞] 發現臺灣目前最古老人類化石  細胞膜的構造
細胞膜的構造  悲傷與快樂的音樂引起不同的腦部活化型態
悲傷與快樂的音樂引起不同的腦部活化型態  頭皮毛囊與精神疾病診斷
頭皮毛囊與精神疾病診斷  白蟻透過腸道微生物高效率獲得能量
白蟻透過腸道微生物高效率獲得能量  細胞凋亡 (Apoptosis)
細胞凋亡 (Apoptosis)  國際生物多樣性日專題 – 何謂生物多樣性?
國際生物多樣性日專題 – 何謂生物多樣性? 
