化學示範實驗:咻聲瓶—氣態乙醇的燃燒(The Combustion of Gaseous Ethanol)
化學示範實驗:咻聲瓶—氣態乙醇的燃燒(The Combustion of Gaseous Ethanol)
國立彰化師範大學化學系學生鄭綉蓉/國立彰化師範大學化學系楊水平副教授責任編輯
前言
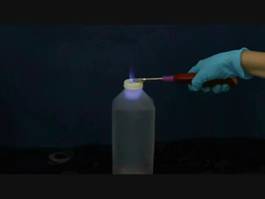
點燃充滿氣態乙醇的塑膠瓶,乙醇瞬間燃燒產生絢麗的火焰和發出尖銳的響聲,創造出驚奇又有趣的效果,讓學生眼睛為之一亮,而且感到不可思議。
示範實驗影片
請按此連結:咻聲瓶—氣態乙醇的燃燒(The Combustion of Gaseous Ethanol),YouTube。
一、示範前準備
1. 取一個含瓶蓋的HDPE瓶,在瓶蓋中間用熱熔槍熔掉、或用大型剪刀或圓式銼刀以插入旋轉方式戳成一個直徑約1.5 cm的圓形孔洞,如圖一所示。
圖一 瓶蓋戳成一個直徑約1.5 cm的圓形孔洞
二、示範咻聲瓶
1. 攜帶戳好瓶蓋孔洞的HDPE瓶、藥用酒精、小燒杯和點火槍到有可遮光的教室上課。
2. 取適量的藥用酒精於小燒杯中(容積約1500 mL的HDPE瓶,約使用8-10 mL的藥用酒精)。
3. 打開瓶蓋,倒入藥用酒精到HDPE瓶中,蓋上瓶蓋。
4. 壓住瓶蓋的孔洞,並劇烈搖晃和轉動此瓶約60秒,促使藥用酒精加快揮發成氣態,而造成瓶內充滿氣態酒精(氣態乙醇)。
5. 倒出多餘的液態酒精到原來的小燒杯中,盡可能地倒乾淨,以免點火之後因殘留過多的液態酒精而燃燒HDPE瓶,造成危險。裝酒精的燒杯必須遠離火源。
6. 放置HDPE瓶於示範桌上,然後關閉電燈,關閉窗簾遮光。
7. 取一把點火槍,產生火焰後,慢慢地靠近瓶蓋的孔洞,如圖二所示。
圖二 點火槍慢慢地靠近瓶蓋的孔洞
8. 當瓶蓋孔洞附近的氣態酒精被點燃後,瓶內的氣態酒精也會瞬間被點燃,突然由瓶蓋孔洞射出巨大火焰以及發出”咻”聲,如圖三至圖五所示。
圖三 剛開始點燃的剎那由瓶蓋孔洞射出的火焰
圖四 氣態酒精燃燒過程中由孔洞射出巨大火焰以及發出”咻”聲
圖五 氣態酒精燃燒結束前由孔洞射出巨大火焰以及發出”咻”聲
9. 氣態酒精燃燒後,請學生觸摸咻聲瓶的溫度,並觀察瓶內是否有液體。
溶液和器材
1. HDPE瓶(含瓶蓋,高密度者才耐高溫,塑膠分類符號2號,約1500 mL容量) 一個
2. 熱熔槍、剪刀(大型)或銼刀(圓式) 一支
3. 藥用酒精(95% 乙醇) 一瓶
4. 小燒杯(50 mL) 一個
5. 點火槍 一把
原理和概念
● 此示範實驗涉及燃燒反應、放熱反應、反應物濃度、反應速率和活化能的觀念。
● 氣態乙醇(氣態酒精)在空氣中燃燒的反應及其燃燒熱,如下反應式所示:
C2H5OH(g) + 3O2(g) → 2CO2(g) + 3H2O(l) ΔHc = -1409.26 kJ/mol
● 在此示範實驗中,氣態乙醇燃燒必須存在氧氣,剛開始在瓶蓋孔洞附近的點火時,由於氧氣的相對濃度高,因此氣態乙醇極快速燃燒。然而,燃燒在瓶蓋孔洞下方時,由於空氣只能從小孔洞進入,此時氧氣的相對濃度低,因此氣態乙醇不是一次全部燃燒,導致燃燒速率慢,造成漸層的燃燒效果。
再者,由於瓶蓋孔洞小,燃燒產生的高熱使二氧化碳氣體和水蒸氣快速膨脹,衝出瓶蓋孔洞而發出尖銳的”咻”聲,造成驚奇的效果。
● 由於氣態乙醇燃燒所需的反應活化能較液體乙醇為低,因此其燃燒速率較快。值得注意:咻聲瓶的氣態乙醇燃燒速率比酒精燈的液態乙醇為快;酒精燈的液態乙醇燃燒速率比酒精塊的膠態酒精為快。
● 焰色會隨著醇類分子含碳的比例不同而異。若以甲醇或乙醇進行示範,則會有產出很快速的”咻”聲,而且有藍色的火焰射出瓶外;若是正丙醇及異丙醇,則聲音相似,而且有藍色及黃色火焰在瓶中”舞動”。
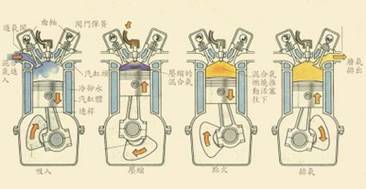
● 此示範實驗的原理與汽車四行程引擎的運作之二個步驟有關:爆炸和排氣。引擎的運作一般分為四個步驟:進氣、壓縮、爆炸和排氣。(1)進氣:活塞往下時凸輪軸會推開進氣閥門,導入汽油和空氣混合形成的混合氣到汽缸內;(2)壓縮:然後關閉進氣閥門,接著活塞上行時會壓縮混合氣;(3)爆炸:當活塞到逹最頂點時火星塞會點火點燃混合氣使其爆炸產生動力,利用混合氣爆炸的力量順勢將活塞往下推;(4)排氣:活塞到逹最低點後接著會往上行,此時凸輪軸會推開排氣閥門,上行的活塞會將燃燒後的癈氣往上推經由排氣閥門排出,完成一次循環,如圖六所示,並詳見參考資料7的網頁動畫。
圖六 汽車四行程引擎的四步驟運作
圖片來源:合興車業,http://www.hersin.com.tw/2009/06/blog-post_08.html
教學提示
1. 示範前也可以事先在咻聲瓶中充滿氣態酒精,用相同大小但無孔洞的瓶蓋蓋緊,然後帶到教室示範。由於部分氣態酒精經過一段時間會冷凝,因此示範前必須再次搖晃,快速換上有孔洞的瓶蓋。最好準備2-3瓶,以防氣態酒精逸失而示範失敗。
2. 燃燒過後的HDPE瓶內會充滿二氧化碳,不能直接重複使用。排除瓶內二氧化碳的有效方法是利用水排出氣體,先在瓶內裝滿水,把水倒出後,瓶子就可重複使用。
3. 醇類皆可進行此示範實驗,它們的性質如下:甲醇:極度可燃、有毒;乙醇:極度可燃、有害;正丙醇:極度可燃、具刺激性;異丙醇:極度可燃、具刺激性。不要使用其他可燃的有機溶液進行此示範實驗。
4. 示範者必須注意安全:(a)盡可能地倒出多餘的液態酒精,以免點火之後因殘留過多的液態酒精而燃燒HDPE瓶,造成危險。(b)點火前瓶蓋必須鎖緊,以免點火之後劇烈反應使瓶蓋爆開飛走,造成危險。(c)為熟練此示範實驗,示範者應該在示範前先用小的HDPE瓶並用少量酒精練習。(d)示範的位置需距離天花板2公尺以上,而且其上不可有易燃物。(e)學生必須距離示範者2-3公尺遠。(f)示範者必須戴上安全眼鏡。(g)示範者必須確定滅火器在可方便取得之處。
5. 示範的瓶子材質除可用HDPE瓶外,亦可用聚碳酸酯瓶(底部有標示PC者),如圖七所示。最好使用一體成形的瓶子。不可為玻璃材質,萬一爆破易發生危險。保特瓶(PET,塑膠分類符號1號)不適用,因它不耐高溫,遇高溫會熔化。
圖七 聚碳酸酯瓶亦適用此示範實驗
圖片來源:Polytech, http://www.polytek-lb.com/product.jhtm?id=1&cid=4
6. 提醒示範者:現場演示示範實驗所展現的變化現象的臨場感,以及激發互動討論的教學效果,比單純的播放影片好很多。
7. 這個示範實驗所使用的溶液和器材均可重複使用,最好裝在一個標示「咻聲瓶—氣態乙醇的燃燒」或放在相似主題的置物箱中備用,方便帶到教室上課。
問題和參考答案
1. 請分別寫出在標準狀況下的甲醇和乙醇燃燒的平衡反應式。
答:甲醇和乙醇的燃燒反應,反應式分別如所下示:
2CH3OH(l) + 3O2(g) → 2CO2(g) + 4H2O(l)
C2H5OH(l) + 3O2(g) → 2CO2(g) + 3H2O(l)
2. 已知液態乙醇的燃燒熱為-1370.7kJ/mol,其蒸發熱為+38.56kJ/mol,試求氣態乙醇的燃燒熱?
答:根據赫士定律(Hess’s law),若一總反應為二個反應之和時,則其反應熱為此二反應熱相之和加。
C2H5OH(l) + 3O2(g) → 2CO2(g) + 3H2O(l) ΔHc = -1370.7 kJ/mol
C2H5OH(l) → C2H5OH(g) ΔHvap = +38.56 kJ/mol
——————————————————————————–
C2H5OH(g) + 3O2(g) → 2CO2(g) + 3H2O(l) ΔHc = -1409.26 kJ/mol
故氣態乙醇的燃燒熱為(-1370.7kJ/mol) – (+38.56kJ/mol) = -1409.26 kJ/mol。
3. 本示範實驗的氣態乙醇燃燒過程中,為何在瓶蓋孔洞附近比孔洞下方的燃燒速率為快?說明其理由。
答:在此示範實驗中,氣態乙醇燃燒必須存在氧氣,剛開始在瓶蓋孔洞附近的點火時,由於氧氣的相對濃度高,因此氣態乙醇極快速燃燒。然而,燃燒在瓶蓋孔洞下方時,由於空氣只能從小孔洞進入,此時氧氣的相對濃度低,因此氣態乙醇不是一次全部燃燒,導致燃燒速率慢,造成漸層的燃燒效果。
4. 燃燒後,瓶底會有少量的液體,這液體主要的成份是什麼?
答:燃燒後產生的液體主要的成份是H2O(l)。
安全
● 示範這個實驗必須戴安全眼鏡及可丟棄的手套。
● 示範這個實驗實行適當的風險評估是老師的責任。
廢棄物處理
● 從咻聲瓶倒出的藥用酒精可重複使用,未使用者可用小瓶子密封裝好。
參考資料(擷取日期:2010年7月)
1. The ‘Whoosh’ Bottle Demonstration, Practical Chemistry, http://www.practicalchemistry.or … tration,240,EX.html.
2. Whoosh Bottle, kitchen table demonstrations, http://www.digitaldapp.org/demos/documents/whooshbottle.pdf.
3. Combustion: Whoosh Bottle Demonstration, http://www.youtube.com/watch?v=SJCcH0ATMQ4.
4. Heat (enthalpy) of Combustion, AUS-e-TURE, http://www.ausetute.com.au/heatcomb.html.
5. Wikipedia-Ethanol (data page), http://en.wikipedia.org/wiki/Ethanol_(data_page).
6. 汽車的動力來源 引擎基本運作原理介紹,合興車業,http://chinese.autoblog.com/2009 … ciple-of-operation/。
7. 四行程柴油引擎的運作原理,U-Car,http://classroom.u-car.com.tw/cl … detail.asp?cfsid=31。







 前一篇文章
前一篇文章 下一篇文章
下一篇文章 化學傳記:法拉第不為人知的一面(六):電磁轉動與電磁感應
化學傳記:法拉第不為人知的一面(六):電磁轉動與電磁感應  不需溶劑的紅血球冷凍保存方法
不需溶劑的紅血球冷凍保存方法  強化玻璃
強化玻璃  【2015諾貝爾化學獎特別報導】DNA修補─為生命提供化學的穩定
【2015諾貝爾化學獎特別報導】DNA修補─為生命提供化學的穩定  【2016年諾貝爾化學獎特別報導】如何將分子變成機器
【2016年諾貝爾化學獎特別報導】如何將分子變成機器  【2014諾貝爾化學獎】如何將光學顯微鏡變成奈米顯微鏡
【2014諾貝爾化學獎】如何將光學顯微鏡變成奈米顯微鏡  【2014諾貝爾化學獎深入報導】 打破光學顯微鏡的解析度極限-超高解析螢光顯微法
【2014諾貝爾化學獎深入報導】 打破光學顯微鏡的解析度極限-超高解析螢光顯微法 
