氫(Hydrogen)的性質
氫(Hydrogen)的性質
國立林口高級中學化學科林明祥老師/國立臺灣大學化學系陳藹然博士責任編輯
地殼中蘊藏最豐富的元素是氧,而宇宙中含量最豐富的元素是氫,氫大約佔據宇宙質量的75%。自然界中,氫元素的分佈也是十分廣泛,不過大多存在於化合物中,如水、石油、碳水化合物蛋白質等有機化合物,而僅少數以氫分子(H2)形式存在。而在恆星上,氫則以電漿態形式存在。
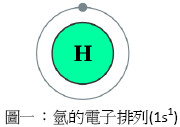
氫是最簡單的元素,原子序為1,位在元素週期表第一位,元素符號為H,其原子質量為1.00794 amu。氫原子本身沒有中子,僅由一個質子與電子構成。
由於氫原子擁有單個電子,所以氫原子容易接受(還原)或失去(氧化)一個電子,氫原子還原生成氫化物(Hydride, H–),反之氫原子氧化形成氫離子(H+),因為氫離子本身沒有中子, H+ 實為質子(Proton)。氫與電負度大的原子(如鹵素、氧和氮)形成化合物時,本身失去電子被氧化,氧化數為+1;相對地,當與電負度小的原子(如金屬)形成化合物時, 本身得到電子被還原,氧化數為 -1。 除了電漿態的物質外,氫離子無法單獨存在晶體或溶液中,這是因為氫離子粒徑小而有極高的正電荷密度,雖然在水溶液中經常以「水合氫離子(H3O+)」來表示 H+,不過這也只是一種理想化的情形,事實上氫離子在水溶液中是以類似於H9O4+ 的形式存在。此外,儘管在地球上少見,H3+ 離子(trihydrogen cation)卻是宇宙中最常見的離子之一。
自然界中,氫有三種同位素,分別為:氕(1H,含量99.985%)、氘(2H,D,含1個中子,含量0.015%)、氚(3H,T,含兩個中子,痕量)。有趣的是,在眾多元素中,氫同位素是唯一各自擁有自己名字的同位素。另一個與其它元素不同的地方,是氫同位素間有很大性質的差異。如重水(D2O)可當核反應中的減速劑;水中若含超過40% D2O即有毒;氚有放射性(半生期約12.32年)。此外,以人工方法合成的氫同位素目前有: 4H、5H、6H、7H。
參考資料
1. 曾國輝,《化學(下冊)第二版》,藝軒圖書出版社,第643頁至第645頁,2001年1月。
2. Albert Stwertka著,劉廣定 增訂,《化學元素導覽》,世潮出版社,第14頁至第17頁,2004年8月。
3. WIKIPEDIA網站–Hydrogen http://en.wikipedia.org/wiki/Hydrogen
4. Cambridge Crystallographic Data Centre網站–Element Name List
http://www.ccdc.cam.ac.uk/products/csd/radii/table.php4
5. 圖一來源:維基百科網站–氫
http://zh.wikipedia.org/zh-tw/Fi … ll_001_Hydrogen.svg
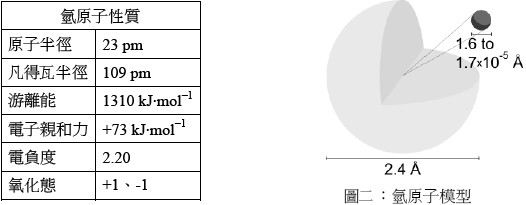
6. 圖二來源:維基百科網站–氫
http://zh.wikipedia.org/zh-tw/File:Hydrogen_atom.svg


 前一篇文章
前一篇文章 下一篇文章
下一篇文章 化學傳記:法拉第不為人知的一面(十):法拉第效應與反磁性
化學傳記:法拉第不為人知的一面(十):法拉第效應與反磁性  【2016年諾貝爾化學獎特別報導】如何將分子變成機器
【2016年諾貝爾化學獎特別報導】如何將分子變成機器 ![[講義] 科學史沙龍:陳竹亭教授、楊信男教授](https://highscope.ch.ntu.edu.tw/wordpress/wp-content/uploads/2015/01/科學史.png) [講義] 科學史沙龍:陳竹亭教授、楊信男教授
[講義] 科學史沙龍:陳竹亭教授、楊信男教授 ![[講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講](https://highscope.ch.ntu.edu.tw/wordpress/wp-content/uploads/2015/10/Aaron-Ciechanover222.png) [講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講
[講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講  目前世界上最精準的時鐘-光晶格光頻原子鐘在低溫環境下的突破
目前世界上最精準的時鐘-光晶格光頻原子鐘在低溫環境下的突破 ![[影音] CASE【百秒說科學】《交叉分子束》](https://highscope.ch.ntu.edu.tw/wordpress/wp-content/uploads/2016/11/CMB-620x280-科學Online.jpg) [影音] CASE【百秒說科學】《交叉分子束》
[影音] CASE【百秒說科學】《交叉分子束》 

文中的氫則以電漿態形式存在
請問什麼是氫的電漿態?
文中的到當與電負度小的原子(如金屬)形成化合物時, 本身得到電子被還原
請問是什麼金屬呢?
請問氫原子可單獨存在嗎?還是會以氫分子存在?
redflyfly您好
您的提問經由責任編輯回應如下:
「因為氫原子活性極大,自然界氫以氫分子存在,只有在高溫等極端環境下才有可能以氫原子態存在」
管理員敬上
請問氫離子與氫原子何者活性大?