胚胎幹細胞(Embryonic stem cell)育成視杯 (optic cup)
胚胎幹細胞(Embryonic stem cell)育成視杯 (optic cup)
台北市立成功高級中學生物科張春梅老師/國立台灣大學動物學研究所陳俊宏教授責任編輯
胚胎幹細胞(Embryonic stem cells,簡稱ES細胞),是從初期胚胎內部細胞團中取得的未分化細胞。它們具有全能分化性(pluripotency),可發育成為人體的220多種細胞類型,但無法獨自發育成一個個體。
眼球的視網膜神經纖維集合為視神經盤(optic disc),由此處形成視神經(optic nerve),穿過脈絡膜和鞏膜而離開眼球。視網膜上的視神經盤因為不具有視覺感光細胞,所以又稱為盲點(blind spot)。視神經盤中央的凹陷部位稱為視杯(optic cup),正常視杯的大小為視神經盤的20-30%。視杯是胚胎發育初期最早形成的視網膜結構,由視杯逐漸發展出感光細胞及神經細胞等,最終形成完整的視網膜構造。
日本神戶理化學研究所生物發生學總合研究中心(RIKEN CENTER FOR DEVELOPMENTAL BIOLOGY (CDB)),由笹井芳樹(Yoshiki Sasai)領導的研究小組,利用小鼠(mouse)的胚胎幹細胞,成功地在試管中培養出胎兒型的眼睛視網膜組織-視杯。此舉乃是再生醫學的重大突破,其論文刊登在2011年4月7日出刊的英國知名期刊《自然》,並被選為該期的封面故事。
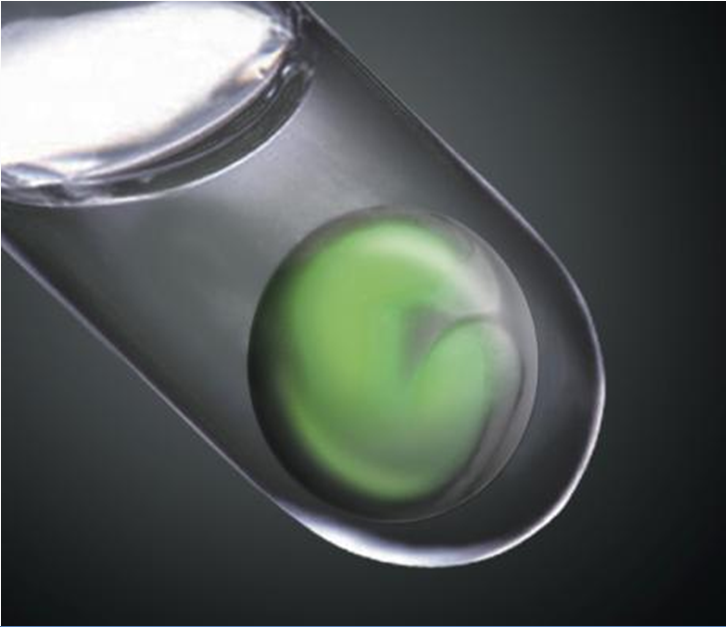
該研究小組運用「三次元自我組織化技術」和SFEBq (serum-free culture of embryoid body–like aggregates)幹細胞培養系統,將小鼠胚胎幹細胞做成細胞凝集塊,放入混合蛋白質和化學物質但不含血清的營養液中培養,持續培養九至十天後,形成初期的眼球視網膜組織(retinal primordium)-視杯。研究人員將視杯的組織再持續立體培養二周左右,形成接近新生小鼠視網膜的組織,不僅包含所有視網膜的主要細胞,還有立體的多層構造,也形成神經細胞間的突觸(圖一)。視網膜是含有多種細胞的複雜構造,在以往的胚胎幹細胞培育技術中,從未培育出如此複雜的組織。研究小組表示,人工培植的視杯結構上與自然形成的差不多,他們將繼續測試它是否能感光,並將相關的神經訊息傳達給大腦。
研究小組一開始是想了解「鄰近組織的訊息交互作用對引導組織形成是否為必要?抑或可自發育中的原型組織自動發生?」並未料到胚胎幹細胞會在培養基中自行運作,形成如此複雜的組織(培養中的幹細胞最初沒有特定形狀,其後會自動發展成有2道外壁的形態,形成視網膜外在及內在的表層。)笹井芳樹表示:「這代表視網膜結構是先天的,細胞擁有製造視網膜的內建資訊(intrinsic self-organizing program)。」
已有眼科專家樂觀地表示:這是醫界的一個重大里程碑,「預估最快5年內就可進行人體試驗」,並期望在10至20年內,人工的視網膜細胞培養技術可臻成熟,讓盲人有機會恢復視力。」這項突破性的技術除了可應用於眼科醫學之外,也可望拓展到其他組織器官的再生研究。
參考資料:
1. 維基百科:胚胎幹細胞 http://zh.wikipedia.org/wiki/%E8 … 9%E7%B4%B0%E8%83%9E
2. Mototsugu Eirak et al., 2011, Self-organizing optic-cup morphogenesis in three-dimensional culture, Nature, vol.472: 51-56.


 前一篇文章
前一篇文章 下一篇文章
下一篇文章 【2014諾貝爾生醫獎特別報導】大腦GPS導航位置與網格細胞系統
【2014諾貝爾生醫獎特別報導】大腦GPS導航位置與網格細胞系統 ![[影音] CASE電影講座:侏羅紀世界─你真的要恐龍復活嗎?](https://highscope.ch.ntu.edu.tw/wordpress/wp-content/uploads/2015/07/ap1.png) [影音] CASE電影講座:侏羅紀世界─你真的要恐龍復活嗎?
[影音] CASE電影講座:侏羅紀世界─你真的要恐龍復活嗎?  憂鬱症治療新契機
憂鬱症治療新契機 ![[講座] 諾貝爾2011年生醫獎得主Dr. Bruce A. Beutler演講](https://highscope.ch.ntu.edu.tw/wordpress/wp-content/uploads/2015/01/2011wk4nk4.png) [講座] 諾貝爾2011年生醫獎得主Dr. Bruce A. Beutler演講
[講座] 諾貝爾2011年生醫獎得主Dr. Bruce A. Beutler演講 ![[講座] 尼安德塔人是什麼樣的人?](https://highscope.ch.ntu.edu.tw/wordpress/wp-content/uploads/2015/02/尼安德塔1.png) [講座] 尼安德塔人是什麼樣的人?
[講座] 尼安德塔人是什麼樣的人? ![[活動] 全球仿生設計競賽-臺灣校園海選](https://highscope.ch.ntu.edu.tw/wordpress/wp-content/uploads/2015/01/z3.png) [活動] 全球仿生設計競賽-臺灣校園海選
[活動] 全球仿生設計競賽-臺灣校園海選  基因銀行(GenBank)
基因銀行(GenBank)  原位雜合技術 (In situ hybridization;ISH)
原位雜合技術 (In situ hybridization;ISH) 
