波以耳定律(Boyle’s Law)
波以耳定律(Boyle’s Law)
台灣師範大學化學系葉名倉教授責任編輯
波以耳(1627-1691)常被尊稱為化學之父,他在1662年為了要了解原子及空間的關係,測量並分析氣體壓力與體積的關係,而提出著名的波以耳定律:定溫下,密閉容氣中的定量氣體之體積與其壓力成反比。你很可能早在小時候,就開始對波以耳定律進行實驗了。當你擠壓汽球時,可以注意到:當你愈用力擠壓它,它似乎就會愈用力地推回來。而當你躺在充氣墊上時,充氣墊被擠壓到某一點時就會停止、不能再被擠壓了。這是因為當你降低某一定量的氣體時,它所產生的壓力會增加。
當兩個變量成反比,如上面例子提到的壓力與體積時,此二變量的乘積將為定值。因為氣體的壓力與體積在定溫下的反比關係,如果你把其中一個的量乘二,另一個的量將會變成原本的一半。從下面的表格可看出氣體的體積與壓力間之反比關係。想像有氣體密閉於鋼瓶之中,而你可以控制它的壓力。注意壓力的變化如何此使體積的值改變,同時這兩個變量的乘積保持一定值(K)。 無論是純質氣體或是混合氣體,波以耳定律皆可應用於求出氣體在另一壓力下的體積。如果你要在實驗室當日氣壓條件下收集一氣體樣本,你很可能會想算出在不同氣壓下此氣體樣本的體積為何。下列的公式可以用來計算在定溫下壓力變化對於體積的影響。 P1V1 = P2V2 其中 P = 壓力 , V =體積 參考資料來源:Science Help Online


 前一篇文章
前一篇文章 下一篇文章
下一篇文章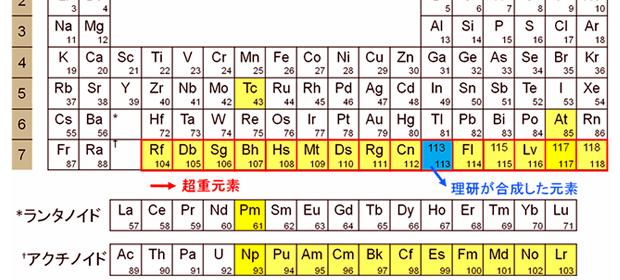 原子序第113超重元素的發現與命名
原子序第113超重元素的發現與命名 ![[新聞] 臺灣年輕團隊成功捕捉「克里奇中間體」與水分子的關鍵化學反應](https://highscope.ch.ntu.edu.tw/wordpress/wp-content/uploads/2015/01/221.jpg) [新聞] 臺灣年輕團隊成功捕捉「克里奇中間體」與水分子的關鍵化學反應
[新聞] 臺灣年輕團隊成功捕捉「克里奇中間體」與水分子的關鍵化學反應  目前世界上最精準的時鐘-光晶格光頻原子鐘在低溫環境下的突破
目前世界上最精準的時鐘-光晶格光頻原子鐘在低溫環境下的突破  化學傳記:法拉第不為人知的一面(九):法拉第和社會的關係
化學傳記:法拉第不為人知的一面(九):法拉第和社會的關係  暖暖包的原理
暖暖包的原理  化學的填字遊戲?
化學的填字遊戲?  【2013諾貝爾獎特別報導】化學獎:將實驗帶入網際空間
【2013諾貝爾獎特別報導】化學獎:將實驗帶入網際空間 
