碳陽離子
碳陽離子 (carbocations)
國立臺灣師範大學化學系碩士班一年級翁于婷研究生
只要有學過有機化學的人,一定知道取代反應(substitution reaction),而講到取代反應就不免牽扯到 $$S_N2$$ 和 $$S_N 1$$ 的兩種反應,兩個反應的反應機構不同,所生出的產物也必然不同,而這個關鍵就在於碳陽離子的形成與否。
碳陽離子 (carbocations) 也叫做碳正離子 (英文為 carbonium ion 或 carbenium ion),這歷史要追朔到 1891 年 G. Merling 團隊的研究,他將溴(bromine)加入到環庚三烯 (cycloheptatriene)並且加熱得到一個晶體 $$\mathrm{C_7H_7Br}$$,卻猜測不出其結構,只知道此化合物具有芳香性 (aromatic)。
1902 年 Norris 和 Kehrman,將無色的三苯甲醇(triphenylmethanol)加入濃硫酸,反應形成深黃色的溶液,也無法確定化合物特性與結構,直到 1902 年 Adolf von Baeyer 確立了這些化合物都具有樣鹽類一般的離子化合物的特性,而開啟了碳陽離子的化學反應。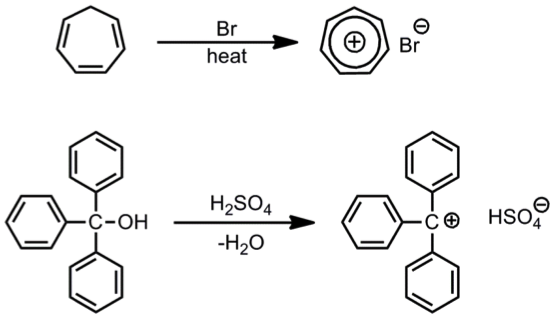
碳陽離子是一個帶正電的碳原子,只鍵結三個不同的原子,而沒有帶任何未鍵結電子(nonbonding electron),所以其價殼層只有 $$6$$ 個電子。碳陽離子的結構是 $$sp^2$$ 混成的平面結構,鍵角成 $$120^\circ$$,形式電荷(formal charge)是 $$+1$$,以結構來看三個鍵共平面,形成平面三角形,而 $$p$$ 軌域垂直於這個平面(Figure 1)。
也正因為碳陽離子只有六個價殼電子,導致他缺乏電子,可以成為路易士酸(Lewis acid)和提供電子對的路易士鹼(Lewis base)反應,在取代反應中更是親電劑 (electrophile)的角色,在 $$S_N1$$ 反應中是決定產物的重要中間體(intermediate),越穩定的碳陽離子就越容易讓親核劑攻擊。
而碳陽離子和自由基(radicals)一樣都是價殼層電子是少於八的缺電子的物種,所以其穩定度就決定於烷基的多寡,烷基可以穩定碳陽離子,原因就在於 $$(1)$$ 誘導效應(inductive effect),$$(2)$$ 是軌域重疊。
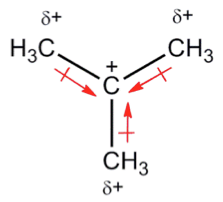
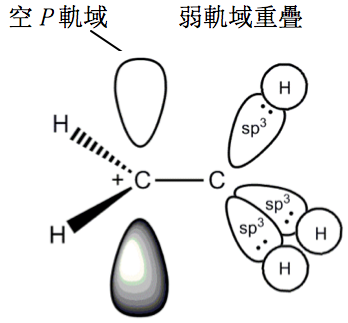
誘導效應是電子透過 $$s$$ 鍵的傳導,將電子集中到碳陽離子上,所以烷基越多電子的誘導效應也越大,碳陽離子穩定度提高(Figure 2)。而軌域重疊度是因為烷基的 $$sp^3$$ 軌域和碳陽離子的空 $$p$$ 軌域會有電子的轉移,這種超共軛(hyperconjugation)的現象,會使碳陽離子的空 $$p$$ 軌域,有電子的重疊,增加碳陽離子的穩定度 (Figure 3) 。
就這兩的原因我們可以得知,當碳陽離子擁有越的的烷基,則其穩定度越好。
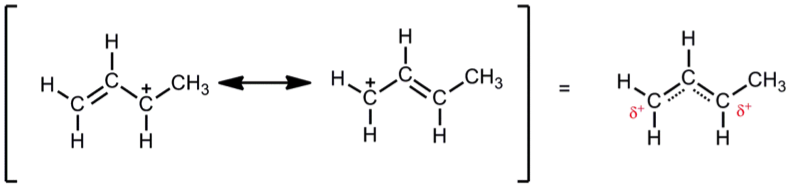
不飽和的碳陽離子,則有共振穩定(resonance stabilization)幫其穩定結構,空 $$p$$ 軌域藉由 $$p$$ 鍵將電子傳遞,比 $$s$$ 鍵效果更好,這種共振未定域化(delocalization)的效果使碳陽離子穩定度更高(Figure 4)。
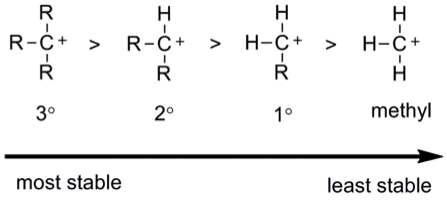
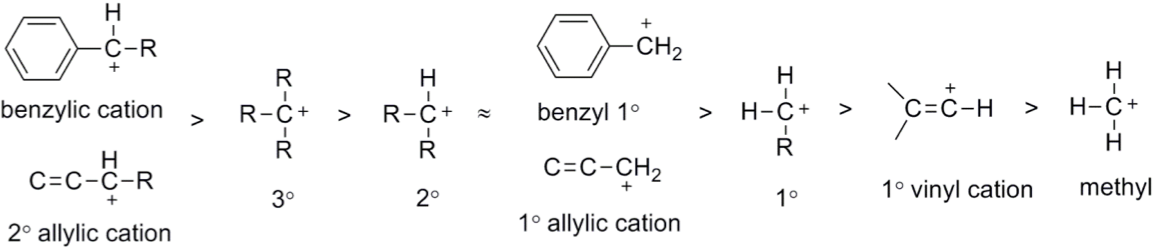
所以,碳陽離子相對穩定度,如下方圖所示,苄基碳陽離子(benzylic cation) 烯丙基碳陽離子(allylic cation)因為電子未定域化,所以最穩定;再來取代基越多超共軛效應越強大的三級和二級碳陽離子;乙烯基碳陽離子(vinyl cation)則是因為,碳碳雙鍵上的碳陽離子是 $$sp$$ 混成,相較於 $$sp^2$$ 混成的碳陽離子更缺電子,所以相對於更不穩定:
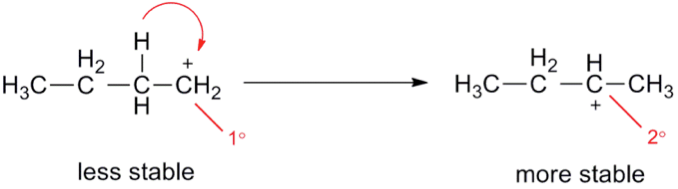
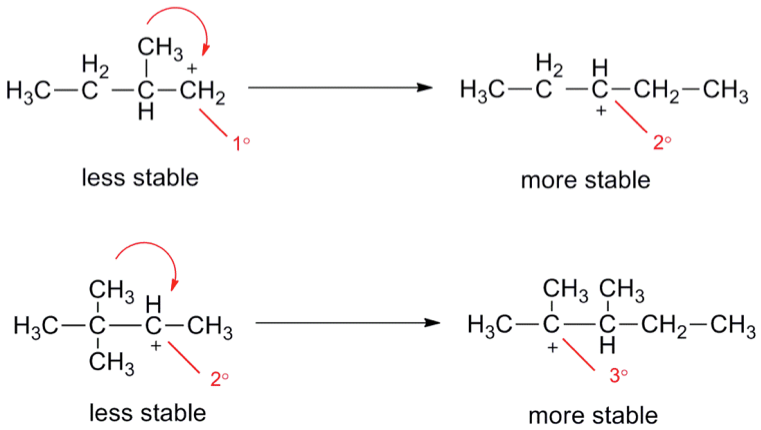
也正因為碳陽離子在不同位置有不同的穩定度,所以碳陽離子就會藉由電子的轉移有重排的現象,我們也發現很多有機反應,碳骨架有重新排列,都是因為反應中間體有碳陽離子形成的關係造成的,較不穩定的碳陽離子會藉由1,2轉移(1,2-shift)重排到較穩定的碳陽離子。而碳陽離子的重排有兩種方式,第一種是氫轉移(hydride shift),第二種是烷基轉移(alkyl shift)。
參考資料
- L. G. Wade, Jr. (2006)。Organic Chemistry. (6th ed.)。Pearson。Chapter 4
- Robert C. Atkins. (2001)。Organic Chemistry. (3rd ed.)。McGraw-Hill。Chapter 3
- Loudon, G, Marc. (1995)。Organic Chemistry. (3rd ed.)。Chapter 4
- WIKIPEDIA。Carbocation。2014.03.19取自http://en.wikipedia.org/wiki/Carbocation
- WIKIPEDIA。tropylium ion。2014.03.19取自http://en.wikipedia.org/wiki/Tropylium_cation



 前一篇文章
前一篇文章 下一篇文章
下一篇文章 【2014諾貝爾化學獎】如何將光學顯微鏡變成奈米顯微鏡
【2014諾貝爾化學獎】如何將光學顯微鏡變成奈米顯微鏡  棉籽粕中殘留的棉籽酚
棉籽粕中殘留的棉籽酚  化學傳記:法拉第不為人知的一面(二):從裝訂工變成大學者
化學傳記:法拉第不為人知的一面(二):從裝訂工變成大學者  原子序第113超重元素的發現與命名
原子序第113超重元素的發現與命名  【2014諾貝爾化學獎深入報導】 打破光學顯微鏡的解析度極限-超高解析螢光顯微法
【2014諾貝爾化學獎深入報導】 打破光學顯微鏡的解析度極限-超高解析螢光顯微法  莫耳和公斤單位的重新定義
莫耳和公斤單位的重新定義  謎樣的分子:克里奇中間體
謎樣的分子:克里奇中間體 
