醇的保護(Protection of Alcohols)
醇的保護(Protection of Alcohols)
國立臺灣師範大學化學系三年級學生趙崇瀚
在一般常見的水溶液化學反應環境中,醇類在羥基上的氫並不是太好的酸 $$(pK_a\approx 16)$$,甚至比水的酸性更低 $$(pK_a=15.7)$$,但比起有機化合中大部分碳上的氫($$pK_a$$ 通常大於 $$20$$)則算是相當酸的氫。
因此,有機反應中羥基的氫的反應性相當的高,換言之,若是一有機分子本身具有多個官能基(包含羥基),則在合成步驟中用來修飾分子的反應試劑可能因為優先與羥基作用,而導致失去原本的功效。最為常見的例子,是使用同時含有鹵素和羥基的分子製作格里納試劑(Grignard reagent),考慮以下例子:
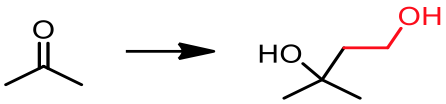
欲從丙酮合成含有兩個羥基的分子
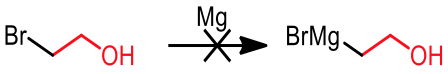
最為常見的合成法是先製備格里納試劑,再對丙酮進行反應。然而在條件下製備格里納試劑時,便會產生問題,並沒有辦法得到理想的反應試劑。
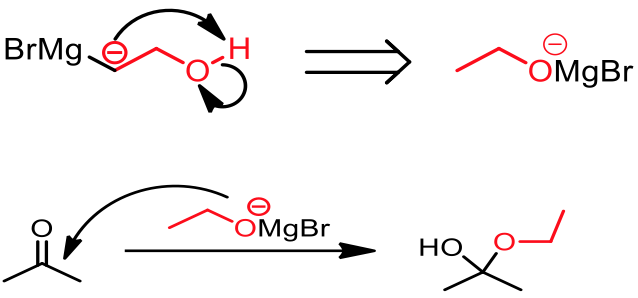
因為格里納試劑本身可視為帶負電的烷基(烷類 $$pK_a=50$$ ,其共軛鹼相當的強),而羥基的氫較烷鏈上的氫還酸,所以此步驟得到的結果其實是 $$\mathrm{OH}$$ 的氫被去質子化之後的產物。如此一來,我們便無法得到理想的產物。
要解決羥基上的氫對試劑造成的干擾,最好的辦法就是將羥基「上保護」。作法是將羥基修飾成反應性較低的基團,等待所有可能會被羥基干擾的反應進行完畢後,再將此反應性低的基團轉變回原來的羥基。
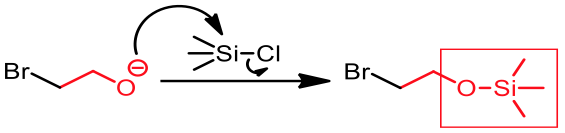
在有機實驗室中,最常用的保護基團是三甲基氯矽烷(trimethylsilyl chloride),而步驟是先主動用鹼拔除羥基的氫,再讓帶有負電的氧去攻擊 $$\mathrm{Si}$$,使得氯離子帶負電離去。此步驟中親核劑攻擊「三級」的受體 $$\mathrm{(Si)}$$ 違反了一般 $$S_N2$$ 反應的原則,然而在此例中因為 $$\mathrm{Si}$$ 較 $$\mathrm{C}$$ 來得大,所以即便是三級的受體,$$\mathrm{C-Si}$$ 之間的化學鍵夠長,能夠讓親核劑有足夠的空間打在 $$\mathrm{Si}$$ 上,進行類 $$S_N2$$ 反應。
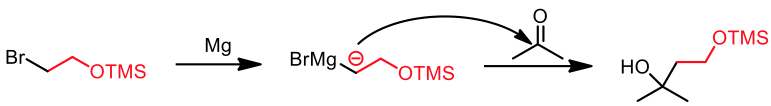
如此一來,受到保護的 $$\mathrm{OH}$$ 便不會干擾格里納試劑的生成
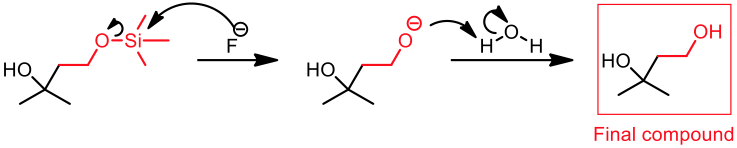
在會受OH干擾的反應進行完畢後(此例中為格里納試劑的親核反應),可將 OTMS 此一基團轉變成原來的 $$\mathrm{OH}$$ 基,最常見的方法是用含有氟離子的鹽類去掉保護,最後就能得到原本所要得到的產物。
之所以選用氟離子來去除保護基,是因為矽和氟具有很強的結合力,能夠形成較穩定的化學鍵。然而,三甲基氯矽烷的 $$\mathrm{O-Si}$$ 鍵並不是非常強,實驗室中在進行管柱層析純化產物時,就有可能將 OTMS 去保護。
所以若要達到較好的保護效果,通常會選用較大的保護基,像是 t-butylchlorodimethylsilane(TBDMSCl)![]() 較不會在純化的過程中就被去保護。
較不會在純化的過程中就被去保護。
在有機合成中,除了製作格里納試劑之外,仍有許多試劑需要先將 $$\mathrm{OH}$$ 基保護住,再進行合成。對 $$\mathrm{OH}$$ 基上保護的用途可說是相當多,在有機合成中,如何靈活運用保護基也是一門重要的課題,僅此只以最為常見的例子作為介紹。
參考資料
- David R. Klein (2012). Organic Chemistry (1st). John Wiley & Sons, Inc
- Wade, L. G. (2013) Organic chemistry Boston : Pearson
- Vollhardt, K. Peter C. (2009) Organic chemistry : structure and function (6th ed.). New York: W. H. Freeman and Company


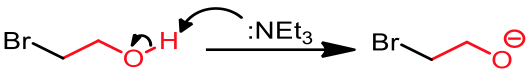
 前一篇文章
前一篇文章 下一篇文章
下一篇文章![[講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講](https://highscope.ch.ntu.edu.tw/wordpress/wp-content/uploads/2015/10/Aaron-Ciechanover222.png) [講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講
[講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講  化學傳記:法拉第不為人知的一面(十):法拉第效應與反磁性
化學傳記:法拉第不為人知的一面(十):法拉第效應與反磁性  【2014諾貝爾化學獎深入報導】 打破光學顯微鏡的解析度極限-超高解析螢光顯微法
【2014諾貝爾化學獎深入報導】 打破光學顯微鏡的解析度極限-超高解析螢光顯微法  化學的填字遊戲?
化學的填字遊戲?  強化玻璃
強化玻璃  莫耳和公斤單位的重新定義
莫耳和公斤單位的重新定義  2014諾貝爾化學獎的遺珠:結構光照明顯微法
2014諾貝爾化學獎的遺珠:結構光照明顯微法 
