血紅素
血紅素 (Heme)
國立臺灣師範大學化學系江宣儀研究生/國立臺灣師範大學化學系葉名倉教授責任編輯
血紅素是由一個大型的有機雜環化合物紫質(Porphyrin),且該環內中心含鐵原子(iron)所組成,為一種含鐵輔基。並非所有的紫質具有鐵原子,但還有紫質的金屬蛋白都以血紅素為輔基,此即為原血紅蛋白(hemeprotein)。原血紅蛋白(hemeprotein)可依據不同的功能加以分類,包含運輸雙原子氣體分子、化學催化、偵測雙原子氣體、及電子傳輸。一般較為討論的為血紅蛋白(hemoglobin),具有含鐵的金屬蛋白質存在於脊椎動物的紅血球中,可將氧氣從肺臟運輸至其他身體的組織。
血紅素能與氧氣結合成氧合血紅素,將氧氣運輸至各組織,同時氧氣與血紅素極易分開,在到達肺部毛細管時,即與氧氣結合成氧合血紅素,但當紅血球到達組織毛細管時,氧馬上與血紅素分開,供給組織,此時血紅素稱為還原血紅素。血紅素同時與二氧化碳結合為二氧化碳血紅素,攜帶二氧化碳氣至肺部排出體外。血紅素在遇一氧化碳氣時,因一氧化碳對血紅素的親和力是氧氣之二百至二百五十倍,故即與一氧化碳結合為一氧化碳血紅素,而排斥氧,故須注意吸入一氧化碳氣。除了紅血球中含有血紅素外,在肌肉內亦存在有血紅素,稱為肌肉血紅素,作用為使肌肉在收縮時壓迫血管,而缺氧時供應氧氣。血紅蛋白(Hemoglobin)是高等生物體內負責運載氧的一種蛋白質。可以用平均細胞血紅蛋白濃度測出濃度。
血紅蛋白化學式:C3032H4816O812N780S8Fe4。人體內的血紅蛋白由四個亞基構成,分別為兩個α亞基和兩個β亞基,在與人體環境相似的電解質溶液中血紅蛋白的四個亞基可以自動組裝成α2β2的形態。
血紅蛋白的每個亞基由一條肽鏈和一個血紅素分子構成,肽鏈在生理條件下會盤繞摺疊成球形,把血紅素分子抱在裡面,這條肽鏈盤繞成的球形結構又被稱為珠蛋白。血紅素分子是一個具有紫質結構的小分子,在紫質分子中心,由紫質中四個吡咯(pyrrole)環上的氮原子與一個亞鐵離子配位結合,珠蛋白肽鏈中第8位的一個組氨酸殘基中的吲哚側鏈上的氮原子從紫質分子平面的上方與亞鐵離子配位結合,當血紅蛋白不與氧結合的時候,有一個水分子從紫質環下方與亞鐵離子配位結合,而當血紅蛋白載氧的時候,就由氧分子頂替水的位置。
血紅蛋白與氧結合的過程是一個非常神奇的過程。首先一個氧分子與血紅蛋白四個亞基中的一個結合,與氧結合之後的珠蛋白結構發生變化,造成整個血紅蛋白結構的變化,這種變化使得第二個氧分子相比於第一個氧分子更容易尋找血紅蛋白的另一個亞基結合,而它的結合會進一步促進第三個氧分子的結合,以此類推直到構成血紅蛋白的四個亞基分別與四個氧分子結合。而在組織內釋放氧的過程也是這樣,一個氧分子的離去會刺激另一個的離去,直到完全釋放所有的氧分子,這種有趣的現象稱為協同效應。
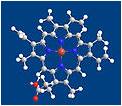
血紅素分子結構
由於協同效應,血紅蛋白與氧氣的結合曲線呈S形,在特定範圍內隨著環境中氧含量的變化,血紅蛋白與氧分子的結合率有一個劇烈變化的過程,生物體內組織中的氧濃度和肺組織中的氧濃度恰好位於這一突變的兩側,因而在肺組織,血紅蛋白可以充分地與氧結合,在體內其他部分則可以充分地釋放所攜帶的氧分子。可是當環境中的氧氣含量很高或者很低的時候,血紅蛋白的氧結合曲線非常平緩,氧氣濃度巨大的波動也很難使血紅蛋白與氧氣的結合率發生顯著變化,因此健康人即使呼吸純氧,血液運載氧的能力也不會有顯著的提高。
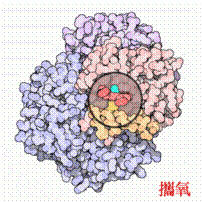
血紅蛋白可動的結構賦予其運送氧的能力
除了運載氧,血紅蛋白還可以與二氧化碳、一氧化碳、氰離子結合,結合的方式也與氧完全一樣,所不同的只是結合的牢固程度,一氧化碳、氰離子一旦和血紅蛋白結合就很難離開,這就是煤氣中毒和氰化物中毒的原理,遇到這種情況可以使用其他與這些物質結合能力更強的物質來解毒,比如一氧化碳中毒可以用靜脈注射亞甲基藍的方法來救治。


 前一篇文章
前一篇文章 下一篇文章
下一篇文章 化學的填字遊戲?
化學的填字遊戲?  化學傳記:法拉第不為人知的一面(五):兩個演講會
化學傳記:法拉第不為人知的一面(五):兩個演講會  【2011諾貝爾化學獎】具有黃金比例的晶體
【2011諾貝爾化學獎】具有黃金比例的晶體  中間體與穩定狀態近似法
中間體與穩定狀態近似法  利用奈米粒子高效率吸收太陽能
利用奈米粒子高效率吸收太陽能  莫耳和公斤單位的重新定義
莫耳和公斤單位的重新定義 
