苯酚(phenol)
苯酚(phenol)
台北市立第一女子高級中學二年級陳虹儒/台北市立第一女子高級中學化學科詹莉芬老師修改/國立台灣師範大學化學系葉名倉教授責任編輯
苯酚基本資料

苯酚的穩定性
苯酚分子是由一個羥基直接連在苯環上構成,為烯醇式結構(如下圖左)。但由於苯環的穩定性,這樣的結構幾乎不會經由電子或化學鍵的轉化為酮式結構(如下圖右)。
苯酚的製備
1.熔融苯磺酸法(最早用於製取苯酚的方法)
(1)苯與濃硫酸經磺化反應後製得苯磺酸
(2)苯磺酸與氫氧化鈉進行熔融反應後產生苯酚鈉與硫酸納
(3)苯酚鈉加酸處理後即得到苯酚
反應流程如下:
2.異丙苯法
(1)苯與丙烯經加成反應後產生異丙苯
(2)異丙苯氧化後製得苯酚
[優點]苯和丙烯屬於廉價的原料,轉化後的苯酚與丙酮則屬較高價值物質。
反應式及流程圖如下:
C6H6+H2C=CHCH3→C6H5CH(CH3)2
C6H5CH(CH3)2+O2→C6H5OH+CH3COCH3

3.氯苯水解法
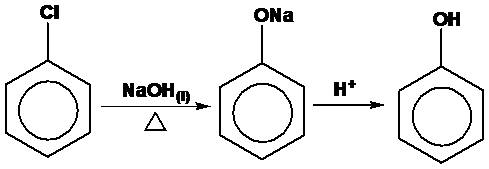
氯苯在氫氧化鈉水溶液中的水解製得苯酚。
反應流程圖如下:
困難]由於氯苯的氯原子參與苯環的共軛,這個水解過程十分困難,需要在高壓(28MPa)、高溫(300℃)、以銅作催化劑的條件下進行。
4.苯胺水解法
苯酚的化學性質及應用
1.苯酚的解離:
此陰離子團可以存在多種共振結構:
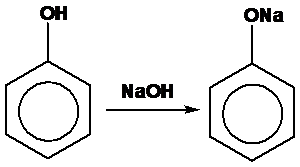
因此苯酚的-OH基的H+是可以解離出來的(Ka僅10-10),與醇類的-OH性質不相同。譬如苯酚可與強鹼進行酸鹼中和反應:
但也由於苯酚酸性太弱,故無法使藍色石蕊試紙變紅,也無法與碳酸氫鈉反應產生CO2
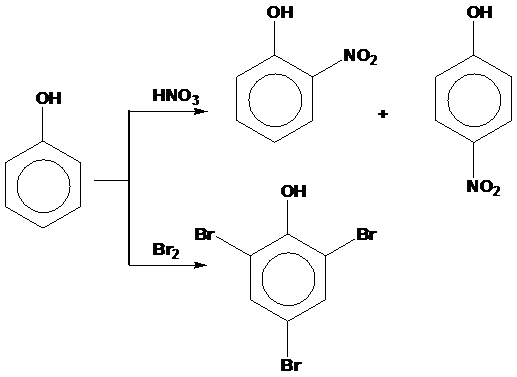
2.苯酚可進行取代反應,依取代不同位置氫原子,可分成兩類:
(1)苯環上進行硝化或鹵化反應,形成溴苯酚等產物,反應流程如下:
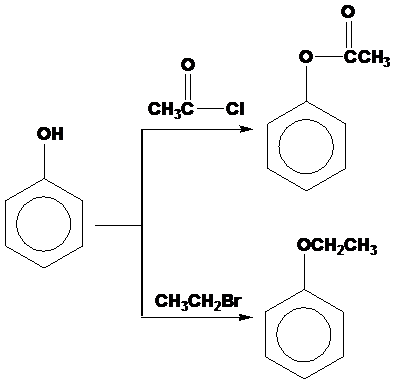
(2)取代反應發生在羥基上,即羥基上之氫原子被碳鍊取代,生成醚類或酯類。
3.苯酚於空氣中會氧化,形成粉紅色的苯醌。
 4.大量製備苯酚與甲醛在酸或鹼的催化下會發生縮合反應,產生網狀聚合物,俗稱電木的酚醛樹脂(Phenolic resin)。這種合成塑料的耐熱性、耐燃性、耐水性和絕緣性優良且易於切割,若在製程中加入不同的材料,還可以得到功能各異的改性酚醛樹脂。
4.大量製備苯酚與甲醛在酸或鹼的催化下會發生縮合反應,產生網狀聚合物,俗稱電木的酚醛樹脂(Phenolic resin)。這種合成塑料的耐熱性、耐燃性、耐水性和絕緣性優良且易於切割,若在製程中加入不同的材料,還可以得到功能各異的改性酚醛樹脂。
5.苯酚與Fe3+可形成紫色錯離子,這也是檢驗苯酚的方法之一。
Fe3++6C6H5OH→H3[Fe(OC6H5)6]+3H+
6.苯酚可作殺菌劑、麻醉劑、防腐劑、外科整型手術之脫皮劑;由於苯酚具有毒性可用於殺菌,外科醫師約瑟夫.李斯特(Joseph Lister)首先將苯酚用於手術是和傷口的消毒,大幅降低了手術後感染的機會,拯救了無數病人的寶貴生命,這位偉大的醫師也因此被尊稱為消毒防腐之父,目前已被其他藥品取代。諷刺的是:救人無數的苯酚也因為它的強烈毒性,被二次大時的納粹用於快速處決集中營裡的囚犯,當時的醫生利用特殊的針頭對囚犯的心臟直接注射高濃度的苯酚,受害者在短暫的時間內便會死亡。
7.苯酚經加工後可合成的化合物:
(1)阿斯匹靈(Aspirin):是目前常見的頭痛藥,還具有抗凝血的作用可防止中風。
阿斯匹靈結構:
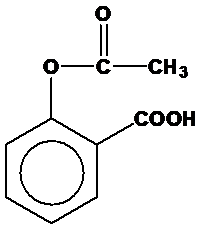
(2)強力炸藥三硝酚:在戰爭中不可或缺的武器
三硝酚結構:
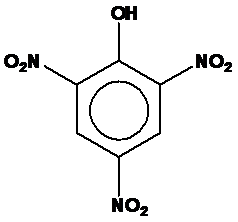
由於這個有趣的巧合,還發生了這樣的故事:二次大戰時,當時世界石炭酸的主要出口來自英國,為因應戰爭需要,英國將所有石炭酸都被製成炸藥投入戰場,造成美國石炭酸的供應短缺,發明大王愛迪生決定自行設計一條製造苯酚的生產線;不料這條生產線的效率太好,除了供應製造酚醛樹脂的原料外還多出許多,德國當局為了阻止這一大批石炭酸變成對德國有威脅的炸藥,便提議由在美國設廠的德國拜耳藥廠將這些原料全數買下作為阿斯匹靈的原料,乍看之下這個提議十分合理且人道,但愛迪生識破了這個陰謀,便將這批石炭酸賣給美國軍方,讓德國的陰謀功敗垂成。
苯酚的毒性
1.苯酚具有強烈毒性,若吸入將刺激鼻咽,甚至影響中樞神經系統
2.食入則會造成口及咽嚴重的灼傷、腹痛、發紺、肌肉虛弱、顫抖、痙攣、腎及肝損害、昏迷及死亡。
3.苯酚及其濃溶液對皮膚有強烈的刺激作用,若不慎將苯酚沾到皮膚上,應用酒精或聚乙二醇清洗;若量較大或者混有氯仿,則需要進行急救。沾到衣服上需用大量水沖洗。
4.由於苯酚的高反應性,酚污染對生態環境傷害很大。
參考資料
1. http://zh.wikipedia.org/zh-tw/%E8%8B%AF%E9%85%9A
2. http://zh.wikipedia.org/wiki/%E9%85%9A
3.4.Joe Schwarcz(2004),「蘇老師掰化學:懂1點化學很有用」,第73~77頁


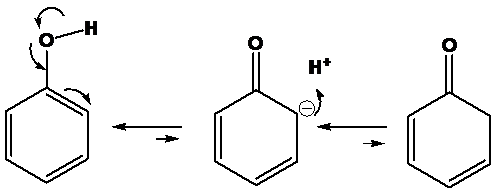
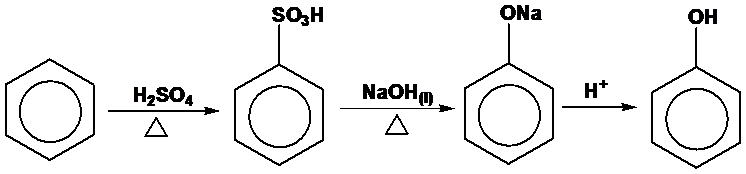



 前一篇文章
前一篇文章 下一篇文章
下一篇文章![[講義] 科學史沙龍:陳竹亭教授、楊信男教授](https://highscope.ch.ntu.edu.tw/wordpress/wp-content/uploads/2015/01/科學史.png) [講義] 科學史沙龍:陳竹亭教授、楊信男教授
[講義] 科學史沙龍:陳竹亭教授、楊信男教授  利用奈米粒子高效率吸收太陽能
利用奈米粒子高效率吸收太陽能  2014諾貝爾化學獎的遺珠:結構光照明顯微法
2014諾貝爾化學獎的遺珠:結構光照明顯微法  化學傳記:法拉第不為人知的一面(十一):凡人法拉第
化學傳記:法拉第不為人知的一面(十一):凡人法拉第  【2013諾貝爾獎特別報導】化學獎:將實驗帶入網際空間
【2013諾貝爾獎特別報導】化學獎:將實驗帶入網際空間  【2019諾貝爾化學獎】鋰離子電池
【2019諾貝爾化學獎】鋰離子電池 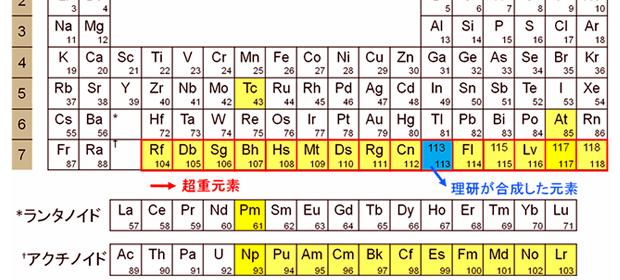 原子序第113超重元素的發現與命名
原子序第113超重元素的發現與命名 
