順反異構物
順反異構物 (Cis-trans isomers)
臺北市立第一女子高級中學二年級張晏如/臺北市立第一女子高級中學化學科周芳妃老師修改/國立臺灣師範大學化學系葉名倉教授責任編輯
順反異構物之結構差異
順反異構物(cis-trans isomers)又稱幾何異構物(geometric isomers,但此種說法已不被IUPAC取用),屬於立體異構物(stereoisomers)的一種。順反異構物形成的主要條件為鍵結在轉動上所受的限制,其中最常見的例子有烯類中的碳碳雙鍵以及環烷類的碳碳單鍵等。
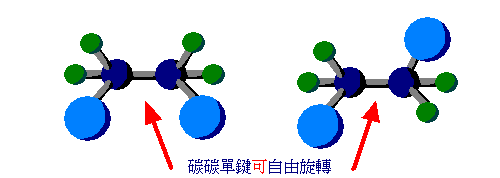
(圖一)中的1,2-二氯乙烷分子中兩個碳原子(深藍)是以單鍵連接。因碳碳單鍵可以自由旋轉(亦即旋轉後與旋轉前的分子結構實為完全相同的分子),所以乙烷不會形成順反異構物。
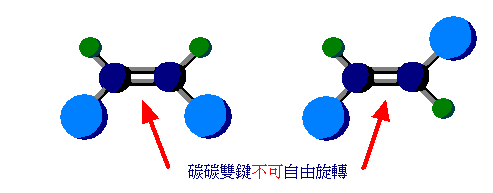
(圖二)中的1,2-二氯乙烯分子中兩個碳原子則是以雙鍵連接。因碳碳雙鍵不可自由旋轉,所以1,2-二氯乙烯可以形成順反異構物。左側的分子中兩氯原子(淺藍)位於雙鍵的同側,屬於順式異構物(順1,2-二氯乙烯);右側的分子中兩氯原子分別位於雙鍵的異側,屬於反式異構物(反1,2-二氯乙烯)。
不屬於順反異構物之例子
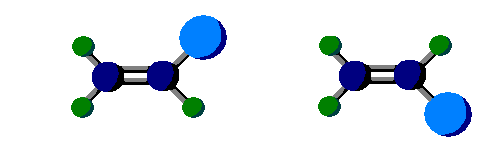
然而,不是所有含有碳碳雙鍵的分子都會形成順反異構物。觀察(圖三)中的左右兩個氯乙烯分子,實際上只是相同的分子翻轉180∘,並不屬於異構物。由此可見,形成順反異構物的條件不只有鍵結在旋轉上受到的限制。另外一個重要的關鍵是雙鍵兩側的碳原子不可有任一同時接上兩個相同的原子或取代基(此例中為氫原子)。若將(圖三)中接兩個氫的碳原子所接的一個氫原子換成氯原子(即(圖二)中的1,2-二氯乙烯)或其他取代基便可以形成順反異構物。
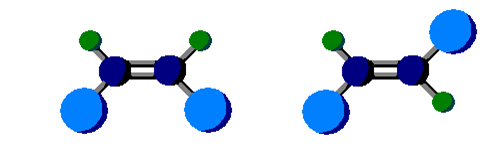
此外,脂環化合物(如環烷類)亦可形成順反異構物。如(圖四)中所示,此種順反異構物的形成原因是環己烷等脂環化合物中的碳碳單鍵之旋轉能力於形成環狀分子後大為受限,導致順反異構物的產生。
總結以上敘述,形成順反異構物的重要條件有二︰(1)鍵結的轉動必須受到限制,以及(2)直鏈中單一碳原子以單鍵連接的取代基比須不同。
順反異構物之物理性質差異
因為結構不同,順反異構物會有不同的物理性質,通常可以從熔點與沸點觀察出來。順式異構物的沸點較反式異構物高,而反式異構物的熔點則較順式異構物高。影響順反異構物中沸點差異的主要因素是極性的存在與否。再以(圖二)中的1,2-二氯乙烯為例,因順反兩分子的組成順序完全相同,其分別於分子間所受的凡得瓦力(Van der Waals dispersion forces)大小相同。然而,在順式分子中帶負電荷的氯離子位於分子的同一側,使得分子的一側微帶負電荷,另一側則微帶正電荷(圖五),順1,2-二氯乙烯因此而屬於極性分子。氯離子分別位於分子異側的反1,2-二氯乙烯則不屬於極性分子(因平均分佈於分子兩側的電荷相平衡)。也正是此種性質使得順1,2-二氯乙烯的分子間吸引力除了凡得瓦力外還另存在偶極─偶極力(dipole-dipole interactions),進而提高破壞分子間作用力所需的能量,也就使得1,2-二氯乙烯的順反異構物中順式分子的沸點較反式分子高。
影響熔點高低的因素則不同於影響沸點的因素。要使固體中分子間作用力發揮最大的效應有一個先決條件︰分子在堆積成固態時需越緊密越好。決定堆積是否緊密的重要因素之一則是分子的對稱性。反式異構物的對稱性較高,分子形狀也較平直,因而較容易緊密堆疊。順式異構物的對稱性則較低,分子容易呈彎曲的「U」形,較不容易緊密堆疊。因此,反式異構物的分子間作用力較順式異構物的分子間作用力有效,破壞其分子間作用力所需的能量也較高,造成反式異構物的熔點較順式異構物高。



 前一篇文章
前一篇文章 下一篇文章
下一篇文章 【2017年諾貝爾化學獎特別報導】將生命捕捉在原子的細節中
【2017年諾貝爾化學獎特別報導】將生命捕捉在原子的細節中  油理油趣─淺談食油的化學
油理油趣─淺談食油的化學  化學傳記:法拉第不為人知的一面(五):兩個演講會
化學傳記:法拉第不為人知的一面(五):兩個演講會 ![[新聞] 臺灣年輕團隊成功捕捉「克里奇中間體」與水分子的關鍵化學反應](https://highscope.ch.ntu.edu.tw/wordpress/wp-content/uploads/2015/01/221.jpg) [新聞] 臺灣年輕團隊成功捕捉「克里奇中間體」與水分子的關鍵化學反應
[新聞] 臺灣年輕團隊成功捕捉「克里奇中間體」與水分子的關鍵化學反應  化學的填字遊戲?
化學的填字遊戲? 

有圖片輔助說明真的比較好懂 謝謝!
邏輯架構清晰
寫得很清楚
“除了凡得瓦力外還另存在偶極─偶極力”
請問偶極偶極力不是屬於凡得瓦力的一種嗎?還是?
謝謝你,解釋清楚!