比爾定律(Beer’s Law)的限制
比爾定律(Beer’s Law)的限制
國立臺灣大學化學系學士生張育唐/國立臺灣大學化學系陳藹然博士責任編輯
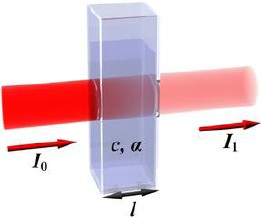
比爾定律,又稱作比爾──朗伯定律(Beer-Lambert Law),是一個光學基礎定律。當光穿透樣品溶液時,光的吸收度(A)與吸收係數(![]() )、光徑長(l)、濃度(c) 三者均呈正比:A=
)、光徑長(l)、濃度(c) 三者均呈正比:A=![]() lc
lc
然而,比爾定律並不適用各種狀況,只適用在某些前提與限制下:
1. 溶液必須是一個均質的溶液,不能存在不均勻的現象。
2. 溶液當中的分子彼此之間不互相作用,例如稀薄溶液。
3. 溶質分子不會因入射光的照射而進行反應。
4. 溶液必須是澄清的,也就是說不能產生散射現象。
5. 僅考慮光的吸收,忽略光的散射、反射等行為。
6. 光源使用單色的平行光。也就是每一束光是相同的波長,且通過相同長度的介質溶液,因為莫耳吸收係數會隨著波長而有所不同。
當測量條件不符合上述前提,以比爾定律計算出的結果就會出現大幅誤差。例如由於濃度的增加,而造成溶液當中組成成分的改變,使得吸光係數並非恆定。例如在水中鉻酸根離子與二鉻酸根離子遵守下列的平衡反應: