標準狀態的基準壓力改變時對熱力學數據的影響(二)
標準狀態的基準壓力改變時對熱力學數據的影響(二)
The effect on thermodynamic data when the standard pressure changed (II)
國立臺灣師範大學化學系兼任教師 邱智宏
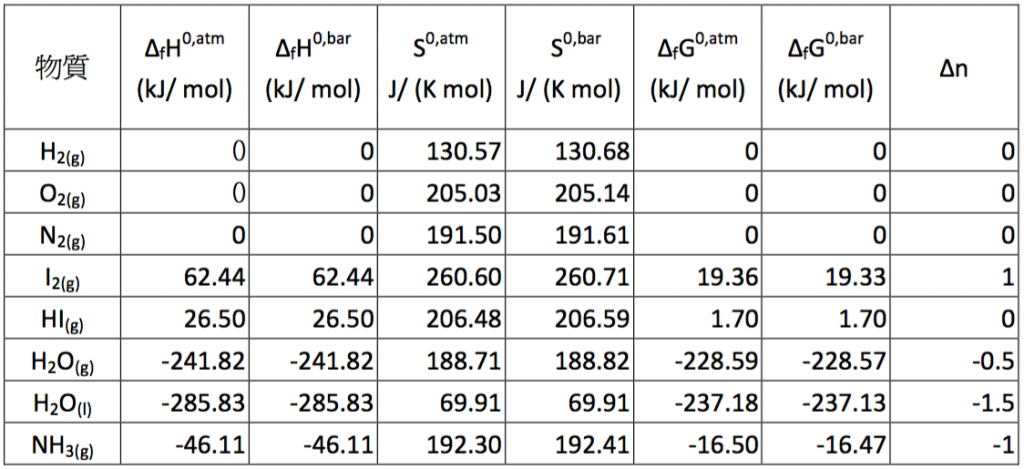
由上表可知,若非作精密計算,基準壓力小幅的改變,對莫耳生成自由能的差異,其實影響甚小。表三中物質的熱力學數據是以 $$1~atm$$ 做為標準壓力,再經公式轉換成以 $$1~bar$$ 為基準,若將此計算得出的數值,直接和物化教科書3上相對應的查表數值相互比較,其相對熵的部分計算值和查表值相差不到萬分之 $$2$$,至於莫耳生成自由能的部分,也小於千分之 $$2$$,基本上若考慮不準度的因素,兩者實際上是相等的,因此上述公式的推導是合乎邏輯的。