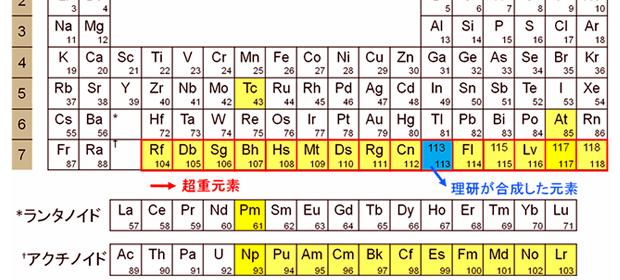
元素
週期表、原子序、鹼金屬、鹼土金屬、鹵素、惰性氣體、主族元素、過渡元素、放射元素、生物物質
[物理史] 氦的發現
氦的發現 (Discovery of Helium)
國立臺灣大學物理學系 楊信男教授、蕭如珀
(譯自APS News,2014年8/9月)
雖然氦在可觀察到的宇宙是第二多的元素,但可由鈾等的放射性元素衰變而生成的氦,在地球上卻是相對稀少。事實上,氦真的太稀少了,所以直到 1868 年才被發現,這主要都要歸功於兩位科學家的努力,一位在英國,另一位在法國。
1859 年,克希何夫 (Gustav Kirchhoff) 認知到可用太陽和其他星球所輻射出的光譜來推斷它們的化學成分。克希何夫使用此方法,發現了銫和銣兩種元素。天文學家對日珥─如火焰般絢麗的氣流,現在已知是稠密氣體的熱雲,的研究尤其感興趣。科學家相信觀察日珥最好的方法是在日食期間。
化學傳記:卡爾.威廉.席勒 (Carl Wilhelm Scheele)
化學傳記:卡爾.威廉.席勒 (Carl Wilhelm Scheele)
國立臺灣師範大學化學系博士生 林欣慧
簡介:
卡爾.威廉.席勒 (Carl Wilhelm Scheele, 1742. 12. 9 – 1786. 5. 21)。是一位瑞典-德國的科學家,最主要的貢獻為發現氧氣、氯氣及鉬 (Molybdenum) 、鎢 (Tungsten) 、鋇 (Barium)。1-3
早期生平:
席勒的父親不是一位成功的商人,在席勒兩歲時家裡就破產了。席勒 14 歲時便到哥特堡在父親的朋友馬汀.安德列亞斯.鮑什 (Martin Andreas Bauch) 所開設的藥房當學徒,在這期間對化學產生濃厚的興趣,閱讀了大量的化學著作及進行了很多化學及藥學的實驗,也因此訓練了他高超的化學實驗技巧,為他未來的研究之路奠下良好的基礎。
原子序第113超重元素的發現與命名
原子序第113超重元素的發現與命名
東京大學理學博士黃郁珊編譯/國立臺灣大學科學教育發展中心陳藹然博士責任編輯
在週期表裡,元素以原子序來排列,原子序代表原子核中的質子數目,具有相同質子數(但不同中子數)的原子有著同樣的化學性質,這些原子稱之為同位素。雖然同位素擁有相同的化性,因為原子核的穩定性不同也因此具有不同的生命長度。質子數低於或等於92的鈾為止都可以從自然界直接發現,比鈾更重的元素是透經由人工合成確認其存在。尤其是原子序104號以上,被稱為超重元素的元素,因為產量極少,難以僅透過化學性質的分析結果來證明新元素的合成,加上所有的超重元素都不安定,會在短時間內衰變為更安定的元素,因此要證明新元素的合成非常重要但又非常困難的一點就在於,確認該元素產生衰變鏈並轉變成已知的較輕原子核。
鈥(Holmium)
鈥(Holmium)
臺北市立永春高級中學一年級錢祥原/台北市立永春高級中學化學科蔡曉信老師
鈥的原子序 $$67$$ 為稀土元素的一種,由瑞典的化學家克利夫(Cleve)於 1878 年所發現(含不純物)。它可從獨居石(Monazite),也稱「磷鈰鑭礦」,化學成分為 $$\mathrm{(Ce, La, Pr, Nd, Th, Y)PO_4}$$ 或矽鈹釔礦 $$\mathrm{((Ce,La,Nd,Y)_2FeBe_2Si_2O_{10})}$$ 中提煉而得。鈥是具有腐蝕性和延展性的銀白色金屬,在乾燥的常溫常壓下較為安定,但它與水及鐵銹容易反應,在空氣中加熱會起燃燒反應,其反應式如下:
$$\mathrm{4Ho+3O_2\rightarrow 2Ho_2O_3}$$
鈥的離子在自然界中幾乎都是以 $$+3$$ 價的狀態存在,而且 $$+3$$ 價的鈥離子也具有像其他稀土離子類似的螢光特性(同時產生其本身獨特的放射光線),且可應用在雷射和玻璃著色劑。
氦氣
氦氣 (Helium)
臺北市立永春高級中學一年級張加樂/臺北市立永春高級中學化學科蔡曉信老師
氦氣(Helium) 的發現是法國科學家皮埃爾·讓森(Pierre Janssen)於 1868 年 8 月 18 日,在印度觀測日全蝕時,碰巧發現的一條特殊光譜線所開始的。同年 10 月 20 日,英國科學家諾曼.洛克耶(Norman Lockyer)也在太陽光譜中發現了一條黃色光譜線,並且提出此物質是存在太陽裡,但當時在地球上尚未發現的元素。後來洛克耶以希臘太陽神 helios 的意涵,將此元素命名為 Helium。
氦氣是位於元素週期表上原子序為 $$2$$ 的元素,為一種惰性氣體,其化學活性極低不易起反應,所以化合物極少且非常不穩定。
氦氣是最難液化的氣體,其沸點只有 $$4.22~K(-268.93^\circ C)$$ ,當其溫度降至 $$2.18~K(-270.97^\circ C)$$ 時性質會改變,黏度會大幅降低,此種狀態稱為超流體(superfluid),超流體狀態的液態氦稱為氦(II)。氦的溶解度也很低,$$20^\circ C$$ 時 $$1~L$$ 的水只能溶解 $$8.61~mL$$。
銥(Iridium)
銥(Iridium)
臺北市立永春高級中學一年級廖秉彥/臺北市立永春高級中學化學科蔡曉信老師
銥是一種化學元素,18 世紀時科學家發現將鉑放入王水中,會產生可溶性鹽類,並會生成少量不可溶的殘留物。英國化學家特南特(Tennant)分析此殘留物,推斷可能有新的金屬元素存在。而後沃克朗(Vauquelin)把殘留物在酸鹼中浸洗,得到一種揮發性氧化物,他認為是新元素的氧化物。後來特南特又大量分析殘留物,而得到兩種新元素,即是鋨和銥兩種元素。
釤(Samarium)
釤(Samarium)
臺北市立永春高級中學一年級陳忠霖/臺北市立永春高級中學化學科蔡曉信老師
簡介:
釤是元素週期表中鑭系元素,原子序為 $$62$$,元素符號為 $$\mathrm{Sm}$$。中等硬度的銀白色金屬,在空氣中容易氧化。釤最常見的氧化數為 $$+3$$,但釤的二價化合物如氧化釤 $$\mathrm{(SmO)}$$、硫化釤 $$\mathrm{(SmS)}$$、硒化釤 $$\mathrm{(SmSe)}$$、碲化釤 $$\mathrm{(SmTe)}$$ 與二碘化釤 $$\mathrm{(SmI_2)}$$ 等亦很常見 ,其中二碘化釤在化學合成上是一種常見的還原劑。釤雖然歸類為稀土元素,但在地殼中是含量排名 $$40$$ 的元素比錫等金屬更常見。釤沒有顯著的生物學反應性,但具有些微毒性。