草酸(Oxalic acid)
草酸(Oxalic acid)
臺北市立第一女子高級中學二年級陳昕慧/臺北市立第一女子高級中學化學科詹莉芬老師修改/國立台灣師範大學化學系葉名倉教授責任編輯
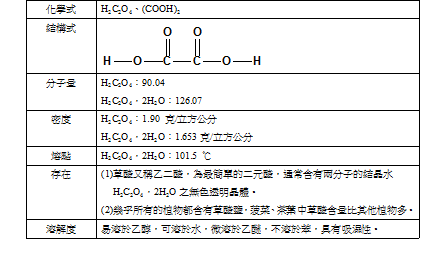
一、草酸的基本性質
二、草酸化學性質及應用
(1)酸性
屬於有機中強酸,Ka1=5.4×10-2,Ka2=5.3×10-5,酸性比乙酸強,可與碳酸鈉(Na2CO3)反應產生CO2。
(2)還原性
具有很強的還原性,能被氧化劑氧化成CO2。
․氧化半反應:C2O42-(aq)→2CO2+2e-
․草酸(或草酸鈉)可使過錳酸鉀(KMnO4)褪色,用於標定過錳酸鉀的濃度。
2MnO4-(aq)+5C2O42-(aq)+16H+(aq)→2Mn2+(aq)+10CO2(g) +8H2O
․由於草酸具有還原力,可作為稻草、麥桿製品的漂白劑。
(3)不穩定性
草酸受熱會分解成CO、CO2、H2O,實驗室可利用此反應製造一氧化碳。
H2C2O4 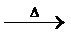 CO+CO2+H2O
CO+CO2+H2O
(4)酯化反應
草酸與醇類進行酯化反應生成酯類,例如草酸和乙醇反應生成草酸二乙酯。
H2C2O4+2C2H5OH→C6H10O4+2H2O
草酸二乙酯結構如下:
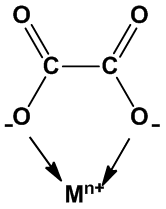
(5)草酸根可做為雙牙基
氧化鐵中的Fe(III)可與草酸根形成水溶性的錯離子,達到除去衣物上鐵鏽沾痕的效果。反應式如下:
Fe2O3+3H2C2O4→2Fe(C2O4)33-+6H+
抗大腸癌藥物oxaliplatin,是一種含草酸根及白金元素的錯合物,進入人體後主要在DNA鏈內或鏈間在G-G與G-A間形成交連的龐大錯化合物。比起原本的藥物Cisplatin,只要較少量即可使 DNA的合成和RNA的轉錄受到抑制。
(6)安全性
草酸也是一種具有腎毒性和腐蝕性的酸性有毒物質,具有非常刺激性的味道。
草酸在人體內不容易被氧化分解,經一連串代謝作用後所形成的產物屬於酸性物質,會導致人體內的酸鹼度失去平衡,長期接觸草酸水溶液可能引發關節痛,身體中過量草酸會與鈣離子結合沈澱造成尿道結石。
(7)用途
在化學工業上可用以製造季戊四醇(C(CH2OH)4,應用於染料工業、製備炸藥)、草酸鈷、草酸鎳、鹼性品綠(別稱孔雀綠,一種染料,禁用殺菌劑)。
鑭系元素(稀土元素)的草酸鹽在很強酸中仍屬難溶鹽,可結晶析出,藉此分離提取之。
塑膠工業則用於生產聚氯乙烯、氨基塑料。
三、草酸的製備
(1)甲酸鈉法
一氧化碳與氫氧化鈉在加壓時反應生成甲酸鈉,然後經高溫(約400℃)脫氫生成草酸鈉,再經鈣化、酸化、結晶及脫水乾燥後,得到成品草酸。
流程如下:
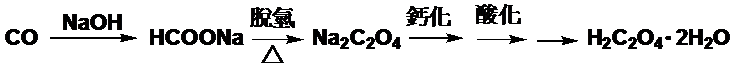
(2)氧化法
以澱粉或葡萄糖、蔗糖為原料,在V2O5為觸媒催化下,以硝酸-硫酸進行氧化反應得草酸。
(3)羰基合成法
一氧化碳經提煉到90%以上,在鈀的催化下與丁醇發生羰基化反應,生成草酸二丁酯,然後經過水解得到草酸。
4 R-OH+4CO+O2 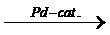 2(CO2R)2+2H2O
2(CO2R)2+2H2O
(CO2R)2+2H2O 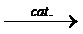 H2C2O4+2R-OH
H2C2O4+2R-OH
草酸二丁酯結構如下(R=C4H9):
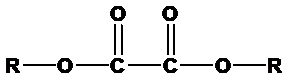
(4)乙二醇氧化法
以乙二醇為原料,在硝酸和硫酸存在下,用空氣氧化而得。
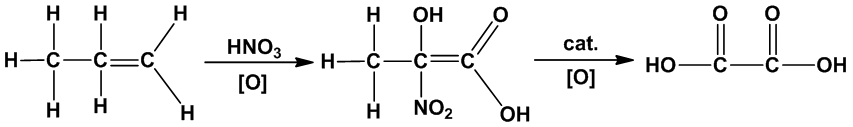
(5)丙烯氧化法
氧化過程分兩步進行。第一步用硝酸氧化,使丙烯轉化為α-硝基乳酸;然後進一步催化氧化得到草酸。第二步也可採用混酸為氧化劑。丙烯氧化法生產工業級草酸二水化合物。
流程如下:
參考資料
1.http://zh.wikipedia.org/zh-tw/%E8%8D%89%E9%85%B8
2.http://en.wikipedia.org/wiki/Oxalic_acid
3.http://baike.baidu.com/view/39573.html?goodTagLemma



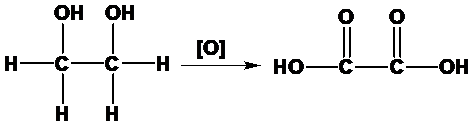
 前一篇文章
前一篇文章 下一篇文章
下一篇文章 化學傳記:法拉第不為人知的一面(四):化學家法拉第
化學傳記:法拉第不為人知的一面(四):化學家法拉第 ![[講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講](https://highscope.ch.ntu.edu.tw/wordpress/wp-content/uploads/2015/10/Aaron-Ciechanover222.png) [講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講
[講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講  2014諾貝爾化學獎的遺珠:結構光照明顯微法
2014諾貝爾化學獎的遺珠:結構光照明顯微法  不需溶劑的紅血球冷凍保存方法
不需溶劑的紅血球冷凍保存方法  利用奈米粒子高效率吸收太陽能
利用奈米粒子高效率吸收太陽能  化學的填字遊戲?
化學的填字遊戲? 
