化學實驗室實驗:銀鏡反應與美感的結合〔I〕
化學實驗室實驗:銀鏡反應與美感的結合(The Silver Mirror Reaction)〔I〕
臺中市立大里高級中學化學科謝孟樺老師/國立彰化師範大學化學系楊水平副教授責任編輯
學生講義
實驗介紹
在鹼性環境中,正一價的銀離子(Ag+)當氧化劑,被還原劑(如甲醛和葡萄糖)還原成銀原子(Ag0),銀原子吸附在玻璃表面即生成銀色的鏡面,稱為銀鏡反應。
銀鏡反應的試劑是在鹼性環境中由硝酸銀或其他銀化合物與氨水混合,生成二氨銀錯離子([Ag(NH3)2]+)的水溶液,此溶液稱為多侖試劑(Tollen’s reagent)。它具有弱的氧化性,一般用於鑑定醛類(aldehyde)的存在。由於多侖試劑保存期短,必須新鮮配製,常見的配製包括兩個步驟:首先,氫氧化鈉溶液加到硝酸銀溶液中,生成棕色的氧化銀(Ag2O)懸浮物,其反應如反應式[1]所示。然後,添加氨水直到所有的氧化銀恰好溶解,生成二氨銀錯離子,其反應如反應式[2]所示。
2AgNO3(aq) + 2NaOH(aq) → Ag2O(s) + 2NaNO3(aq) + H2O(l) [1]
Ag2O(s) + 4NH3(aq) + H2O(l) → 2[Ag(NH3)2]+(aq) + 2OH–(aq) [2]
當進行銀鏡反應時,醛類(RCHO)與二氨銀錯離子反應,生成金屬銀和羧酸根離子(RCOO–),其反應如反應示[3]所示。
RCHO(aq) + 2[Ag(NH3)2]+(aq) + 3OH–(aq) →
RCOO–(aq) + 2Ag(s) + 4NH3(aq) + 2H2O(l) [3]
反應物為甲醛(HCHO),產物為甲酸根離子,其反應如反應式[4]所示。
HCHO(aq) + 2[Ag(NH3)2]+(aq) + 3OH–(aq) →
HCOO–(aq) + 2Ag(s) + 4NH3(aq) + 2H2O(l) [4]
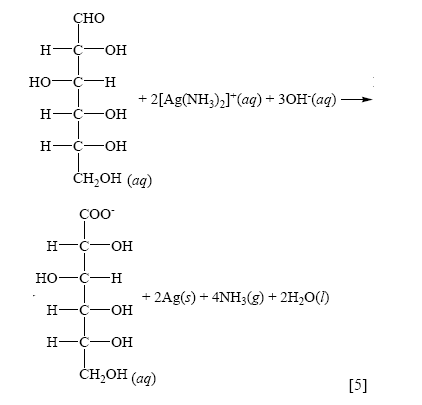
基本上,所有的單糖和部分雙糖為具有還原性的還原醣,也可作為銀鏡反應的還原劑。在水溶液的狀態下,具有醛基(-CHO)或者鄰接碳有羥基(-OH)的酮基(-C=O)之還原醣會形成開鏈(open chain)的結構,這樣的醣類能夠當成還原劑,被二氨銀錯離子氧化。本實驗即是利用葡萄糖的還原性進行銀鏡反應,其反應如反應式[5]所示。
藥品和器材
1. 0.6 M硝酸銀溶液(aqueous AgNO3) 約20 mL/組
2. 2.5 M氫氧化鈉溶液(aqueous NaOH) 約20 mL/組
3. 15 M濃氨水(conc. NH3) 約50 mL/組
4. 10%葡萄糖水溶液(aqueous C6H12O6) 約10 mL/組
5. PE滴管 4支
6. 精緻的附蓋(含塑膠內襯)玻璃瓶 (依實際需求/組)
7. 飾品、彩繪用品 (依實際需求/組)
8. 16 M濃硝酸(conc. HNO3) (依實際需求/組)
安全注意事項
● 本實驗所使用的硝酸銀,照光後會進行光化學反應而生成黑色的銀原子附著衣物或皮膚上,因此必須戴安全眼鏡及可丟棄的手套,也應該穿實驗衣。
● 銀氨溶液應新鮮配製,以避免生成爆炸性的銀(fulminating silver,可能為AgONC或Ag3N)。銀鏡反應後的廢液也應該立即於標示「銀鏡反應廢液」桶中,由老師進一步處理。
● 濃氨水有刺激性,應該放置在抽風櫃中或裝在點滴瓶內,使用時務必小心。
● 若對實驗的安全問題有任何質疑,請勿猶豫,立刻詢問老師。
● 不慎接觸藥品,應該用大量水沖洗,必要時報告老師。
實驗步驟
一、事前準備
1. 事先以量筒測量玻璃瓶的容量大小,依照下面的玻璃瓶容量與藥品使用量進行銀鏡反應,若玻璃瓶的容量大小非下面所列,則可以依照比例關係計算。本次實驗使用25 mL容量的玻璃瓶。
● 25 mL容量的玻璃瓶:1 mL的硝酸銀溶液、0.6 mL的氫氧化鈉溶液、約2 mL的濃氨水(依實際需要)和0.2 mL(4滴)葡萄糖水溶液。
● 50 mL容量的玻璃瓶:2 mL的硝酸銀溶液、1.2 mL的氫氧化鈉溶液、約4 mL的濃氨水(依實際需要)和0.4 mL(8滴)的葡萄糖水溶液。
● 100 mL容量的玻璃瓶:4 mL的硝酸銀溶液、2.4 mL的氫氧化鈉溶液、約8 mL的濃氨水(依實際需要)和0.8 mL(16滴)的葡萄糖水溶液。
2. 已裝過飲料或酒類的玻璃瓶內含乾的殘留物而不易清洗乾淨,實驗前瓶內事先裝滿清潔劑和水浸泡數天,然後在實驗當天用超音波震盪器清洗乾淨,再用蒸餾水潤洗,否則銀鏡會有污點而無法製作完美無缺的飾品。
二、進行銀鏡反應
1. 在一個精緻的玻璃瓶(容量25 mL)內,加入1 mL的0.6 M硝酸銀溶液,再加入0.6 mL的2.5 M氫氧化鈉溶液,混合均勻,如圖一所示。
2. 逐滴地加入15 M濃氨水於玻璃瓶內,並且搖動使其混合反應,直到沉澱物恰好完全溶解,如圖二所示。
3. 以滴管加入4 滴的10%葡萄糖水溶液,蓋上瓶蓋搖晃玻璃瓶,約一分鐘瓶身逐漸析出金屬銀,約五分鐘後「銀鏡」就會現身了!如圖三所示。
4. 反應後瓶內的溶液應盡速倒入於標示「銀鏡反應廢液」桶中。然後,以小量的蒸餾水潤洗,務必完全地清洗掉瓶內的褐色固體物,如圖四所示。
5. 以傾斜倒立方式,促使瓶內的蒸餾水流乾。等待瓶內無水分之後,蓋緊瓶蓋。
6. 在鍍銀的玻璃瓶上黏貼貼紙、彩繪裝飾成為漂亮的飾品,如圖五所示。
廢棄物處理
● 反應後瓶內的溶液應盡速倒入於標示「銀鏡反應廢液」桶中。此廢液含銀離子應該回收再利用,由老師進一步處理。
觀察紀錄
1. 寫出此實驗的各變化過程。
2. 說明各變化過程的化學原理(最好以反應式描述)。
3. 以照片呈現你的實驗結果(漂亮的玻璃品飾物)。
問題
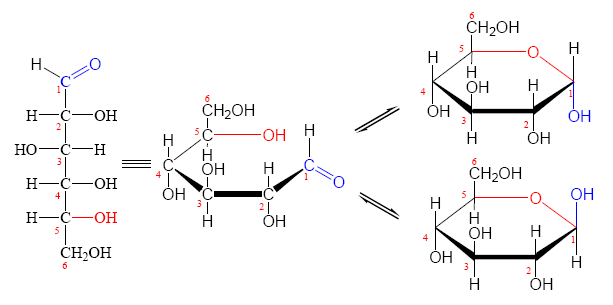
1. 葡萄糖是自然界分布最廣且最為重要的一種單醣,在水溶液中葡萄糖呈現三種不同的形式,而且三者之間達到平衡狀態。其一分子為開鏈狀,如圖六的左邊和中間的結構式所示。另二者是藉由5號碳的羥基(-OH)攻擊接合到1號碳,而形成六員環狀的結構,如圖六的右邊兩個結構式所示。若在環狀結構中第一個C與第二個C上的OH在同側,此分子被稱為α-D-吡喃葡萄糖;若在環狀結構中第一個C與第二個C上的OH在異側,此分子被稱為β-D-吡喃葡萄糖。事實上,在水溶液中開鏈狀葡萄糖的含量非常低(少於於1%),試問在如此低含量的情況下,為何還可以進行銀鏡反應?
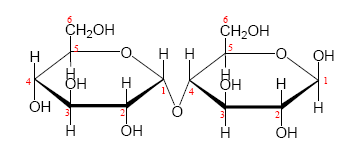
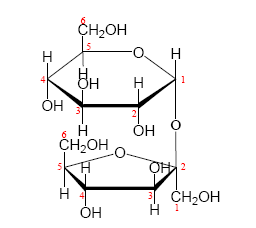
2. 雙醣是一種碳水化合物,由兩個單醣分子經縮合反應脫去一個水分子而生成。圖七和圖八分別為麥芽糖與蔗糖的環狀結構式(紅色數字標明碳數編號)。試由結構式解釋,說明麥芽糖是還原醣,而蔗糖不是還原醣。
3. 本實驗是否可以使用蜂蜜取代葡萄糖當作還原劑來進行銀鏡反應?並說明原因。
4. 若想要洗去鍍好的銀層,可使用適量的稀硝酸(約3 M)處理。試寫出金屬銀溶於稀硝酸的反應式。







 前一篇文章
前一篇文章 下一篇文章
下一篇文章![[講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講](https://highscope.ch.ntu.edu.tw/wordpress/wp-content/uploads/2015/10/Aaron-Ciechanover222.png) [講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講
[講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講 ![[影音] CASE【百秒說科學】《交叉分子束》](https://highscope.ch.ntu.edu.tw/wordpress/wp-content/uploads/2016/11/CMB-620x280-科學Online.jpg) [影音] CASE【百秒說科學】《交叉分子束》
[影音] CASE【百秒說科學】《交叉分子束》 ![[講義] 科學史沙龍:陳竹亭教授、楊信男教授](https://highscope.ch.ntu.edu.tw/wordpress/wp-content/uploads/2015/01/科學史.png) [講義] 科學史沙龍:陳竹亭教授、楊信男教授
[講義] 科學史沙龍:陳竹亭教授、楊信男教授  不需溶劑的紅血球冷凍保存方法
不需溶劑的紅血球冷凍保存方法  化學傳記:法拉第不為人知的一面(十一):凡人法拉第
化學傳記:法拉第不為人知的一面(十一):凡人法拉第  【2011諾貝爾化學獎】具有黃金比例的晶體
【2011諾貝爾化學獎】具有黃金比例的晶體  棉籽粕中殘留的棉籽酚
棉籽粕中殘留的棉籽酚 
