化學情境試題:考古學家的碳-14測年法(Carbon-14 Dating in Archaeology)〔I〕
化學情境試題:考古學家的碳-14測年法(Carbon-14 Dating in Archaeology)〔I〕
台中縣立大里高級中學化學科謝孟樺老師 / 國立彰化師範大學化學系楊水平副教授責任編輯
在回答問題之前,首先請你閱讀與本試題有關的情境描述,以增加你對本試題背景知識的瞭解;然後思考問題解決的策略,並且寫下你的答案;最後用我們提供的參考答案檢查你的答案是否正確。
情境描述
當人們看見一件很古老的物品,最常見的疑問是「這是幾年前的古物?」,考古學家和你一樣,也很想知道古物到底有多古老(圖一)。隨著科技的日新月異,考證年代的技術越來越多,也越來越精準,但是在諸多的方法之中,以「碳-14測年法(carbon-14 dating)」最為普遍,此方法係在1948年由一位曾從事原子彈研究的芝加哥大學里比(W. F. Libby)及其同事所發現。這使考古學家與地球科學家大幅擴展對過去歷史的認知,也由於這項卓越貢獻,因而獲頒諾貝爾化學獎。

圖一 考古學家挖掘古物
圖片來源:Wessex Archaeology, http://www.flickr.com/photos/wessexarchaeology/51572936/
自然界中存在三種碳的同位素,分別為碳-12、碳-13及碳-14,在地球上有98.89%的碳以碳-12的形式存在,有大約1.11%的碳以碳-13的形式存在,只有10-10%是以碳-14存在大氣中。放射性元素碳-14的形成,乃是透過各種宇宙射線與地球外層大氣撞擊而產生的中子,再與大氣中的氮原子作用,釋放出質子。碳-14經由β衰變會逐漸蛻變成氮,蛻變的速率為約每5730年放射性活性減少一半,我們稱這種遞減所需的時間為「半衰期(t1/2)」,如圖二所示。
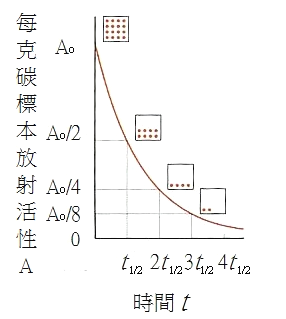
圖二 放射活性與半衰期的關係
碳-14與氧結合生成二氧化碳(14CO2),與普通的不具放射性的碳-12(12CO2)共存於地球大氣和水中,為生物所吸收:植物吸收二氧化碳作為光合作用的原料,各種動物及人類又以植物為食物,因此在所有進入生物體內的碳元素中便存有少量的碳-14,生物體藉由呼吸或光合作用,隨時補充蛻變掉的碳-14,其放射性活性(A0)乃保持與大氣平衡的狀態;一旦生物體死亡,與大氣停止交換,體內碳-14放射性活性(A )就按指數規律減少,在已知碳-14的半衰期(t1/2)下,藉由測量 與 的值,就能定出生物體從死亡至今的絕對年代(t)。放射性活性與衰變時間的關係式如下所示:
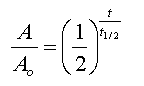
情境試題
1. 已知各種碳同位素原子量分別為:12C = 12.0000 amu,13C = 13.00335 amu,14C = 14.00317 amu,試求碳的平均原子量。
2. 根據「情境描述」,回答下面的問題。
(1) 請寫出放射性元素碳-14形成的核反應式(必須標示元素的質量數合原子序)。
(2) 碳-14經β衰變後的產物為氮,試敘述氮-14原子的內部含有中子、質子和電子的數量各為多少?
3. 考古學家發現非洲洞穴中一處火堆餘燼,測得每公克碳標本每分鐘碳-14衰變3.1次,假設由新鮮木頭缺口測得衰變速率為每克碳標本每分鐘碳-14衰變13.6次(此衰變用大氣中碳-14含量的改變作校正),試求此火堆餘燼的年代。
連結:考古學家的碳-14測年法(Carbon-14 Dating in Archaeology)〔II〕
參考資料(以下網頁擷取日期:2010年2月)
- Carbon dating, Wikipedia, http://en.wikipedia.org/wiki/Carbon_dating.
- 碳十四測年法,國立台灣史前博物館,http://www.nmp.gov.tw/enews/no17/page_04.html。
- 楊進榮、姜樂義, 1987年9月,碳-14定年實驗室又誕生了!─碳-14定年法及其應用,科學月刊,第213期。


 前一篇文章
前一篇文章 下一篇文章
下一篇文章 化學傳記:法拉第不為人知的一面(七):影響法拉第的宗教與人們
化學傳記:法拉第不為人知的一面(七):影響法拉第的宗教與人們  不需溶劑的紅血球冷凍保存方法
不需溶劑的紅血球冷凍保存方法 ![[講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講](https://highscope.ch.ntu.edu.tw/wordpress/wp-content/uploads/2015/10/Aaron-Ciechanover222.png) [講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講
[講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講  化學的填字遊戲?
化學的填字遊戲?  【2017年諾貝爾化學獎特別報導】將生命捕捉在原子的細節中
【2017年諾貝爾化學獎特別報導】將生命捕捉在原子的細節中  【2016年諾貝爾化學獎特別報導】如何將分子變成機器
【2016年諾貝爾化學獎特別報導】如何將分子變成機器  強化玻璃
強化玻璃 
