乙二醇(Ethylene Glycol)
乙二醇(Ethylene Glycol)
台北市立第一女子高級中學二年級黃郁蘋//台北市立第一女子高級中學化學科周芳妃老師修改/國立台灣師範大學化學系葉名倉教授責任編輯
乙二醇的性質
乙二醇(Ethylene Glycol,Monoethylene glycol,簡稱MEG)學名為1,2-乙二醇(Ethane-1,2-diol),分子式為C2H4(OH)2,乙二醇的物性為無色、無臭、有甜味液體,其密度1.11 g/cm3;、熔點與沸點分別為−12.9 °C (8.8°F)及197.3 °C (387°F)。乙二醇易溶於水,可以任意比例與水混合均勻。乙二醇也是易燃性的液體,在110°C以上有爆炸的危險。
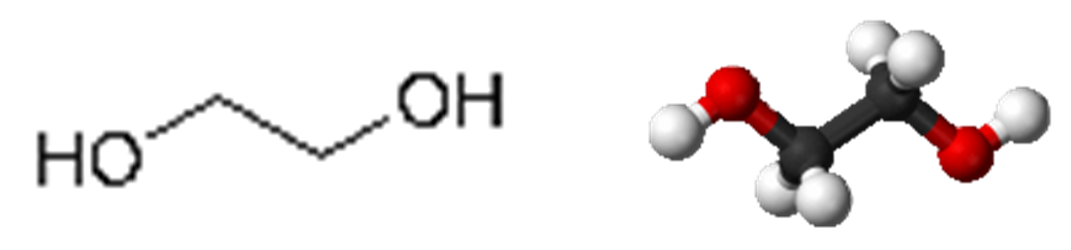
圖片來源: http://encyclopedia.thefreedictionary.com/Ethylene+Glycol
乙二醇的製造
環氧乙烷可在60°C的環境下由稀硫酸催化和大量的水反應成乙二醇
![]()
乙二醇的用途
乙二醇可用來當作汽車引擎抗凍劑或筆記型電腦內的冷卻劑,也可用於除去擋風玻璃上的結冰。乙二醇也是重要的化工原料,可用於聚酯纖維例如聚對苯二甲酸乙二酯(ethylene terephthalate)、樹酯或塑膠飲料瓶(PET)的製造。較細微的用途在於電容器的製造,用來防止筆記型電腦內的液體冷卻系統受到腐蝕。乙二醇在實驗室用途也很多,可用來沉澱蛋白質,這經常是分餾、洗淨和結晶的中間過程之一。它能在有機合成反應中阻止功能小組受反應。乙二醇也是一種在學校內作標本時常使用的防腐劑,被認為比甲醛更安全,但仍需注意安全性。由於乙二醇沸點高於水,對水也有高親和力,使其成為在天然氣製造過程中的理想乾燥劑。有時也用於一些疫苗的製造。鞋子的上光劑、某些墨水或顏料也有大約1~2%左右的乙二醇。也可用於樹木腐爛或發霉的預防與治療。
乙二醇的毒性
具甜味,誤食後會出現興奮、頭暈、頭疼、神智不清,一段時間後,乙二醇被身體分解為乙醇醛(glycolaldehyde),乙醇醛氧化後變為乙醇酸(glycollic acid)
,後為乙醛酸(glyoxylic acid),最後為草酸(oxalic acid)。這些物質將導致心跳過快、高血壓、過度換氣、新陳代謝的酸中毒和腎衰竭。草酸則會與鈣反應成腎結石。
乙二醇的應用史
在1859年,乙二醇首先被法國化學家查爾斯(Charles-Adolphe Wurtz)用來生產冷卻劑和炸藥的成分之一。而直到1937年它的其中一種組成成分環氧乙烷(ethylene oxide)取得容易且價格便宜時,才開始普遍生產。
參考網址:
1. http://encyclopedia.thefreedictionary.com/Ethylene+Glycol


 前一篇文章
前一篇文章 下一篇文章
下一篇文章 油理油趣─淺談食油的化學
油理油趣─淺談食油的化學 ![[講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講](https://highscope.ch.ntu.edu.tw/wordpress/wp-content/uploads/2015/10/Aaron-Ciechanover222.png) [講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講
[講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講  【2016年諾貝爾化學獎特別報導】如何將分子變成機器
【2016年諾貝爾化學獎特別報導】如何將分子變成機器  【2017年諾貝爾化學獎特別報導】將生命捕捉在原子的細節中
【2017年諾貝爾化學獎特別報導】將生命捕捉在原子的細節中  化學傳記:法拉第不為人知的一面(十):法拉第效應與反磁性
化學傳記:法拉第不為人知的一面(十):法拉第效應與反磁性  不需溶劑的紅血球冷凍保存方法
不需溶劑的紅血球冷凍保存方法  莫耳和公斤單位的重新定義
莫耳和公斤單位的重新定義 
