自然界中的金屬螯合作用(Chelation in nature)
自然界中的金屬螯合作用(Chelation in nature)
國立臺灣師範大學附屬高級中學化學科陳昭錦老師
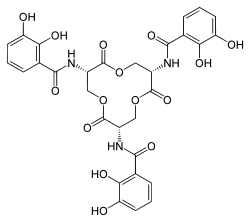
就生物化學及微生物領域而言,所有的金屬酶其特徵均為金屬與肽或輔基螯合,像血紅素及葉綠素中的紫質環都屬於這類的螯合劑。細菌與其宿主都需吸收微量元素來維持生長,例如鐵是細菌許多必需酵素的輔酶,細菌須吸收它才能啟動這些酵素催化細菌所需的生化反應,以維持存活生長。細菌為了跟宿主競爭環境中少量的鐵,會合成及釋放一種低分子量、對鐵有高親和力的化合物,稱為螯鐵蛋白(Siderophore)。其中Enterobactin是目前已知最強的水溶性鐵離子螯合基,其結構如圖一所示。
在地球科學領域中,有機螯合劑如肽及醣類,將金屬離子從礦物或岩石中攫取出來被視為化學風化的主因。環境及自然界中大部分的金屬錯合物都以某些螯合環的形式被縛著,因此土壤中金屬的移動、植物與微生物體內金屬的攝入與累積,都與金屬螯合物有關。許多生化物質都有溶解出特定金屬陽離子的能力,對多數金屬離子而言,蛋白質、多醣類以及多核苷酸等都是很好的多牙配位基。如穀胺酸、組胺酸等胺基酸,如蘋果酸與檸檬酸等有機酸,植物螯合素及金屬含硫蛋白等,也都是典型的螯合劑。
植物可經由吸收累積之過程來移除土壤中之重金屬,在植物忍受與隔離重金屬危害的機制中,金屬硫蛋白(Metallothionein, MT)與植物螯合素(Phytochelatins, PCs)扮演了相當重要的角色。植物螯合素和金屬含硫蛋白是一群可與重金屬結合的蛋白質,當植物體遭受重金屬刺激時便會大量合成。這種受重金屬誘發的金屬含硫蛋白,也證實存在於動物及真菌中,而且同樣在抗重金屬逆境上扮演重要角色。
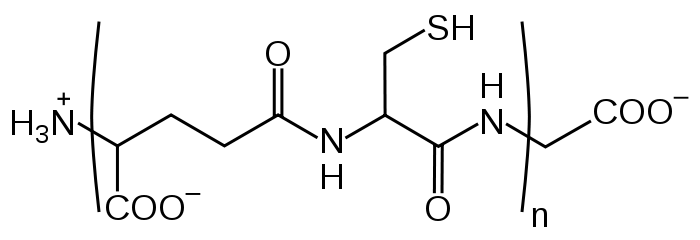
典型的金屬硫蛋白具有61-74個胺基酸,每一個金屬硫蛋白可以結合七個二價離子如鎘、鉻、鋅等。植物螯合素則主要由榖胱甘肽(glutathione, GSH)所構成,如圖二所示,它可以保護植物細胞減少氧化逆境傷害(oxidative stress damage),例如由鎘所引起的脂質過氧化反應。GSH同時也是植物螯合胜肽(phyto-chelations peptides,簡稱PCs)的前驅物。當金屬離子侵入細胞時,會破壞胞內酵素,這時植物螯合胜肽會和金屬離子結合形成螯合物,之後再將這些金屬螯合物運送到液胞中加上硫形成較穩定的結構,以解除金屬毒害。
針對特定重金屬的選擇性螯合作用也可應用在生物復育(bioremediation)方面,這是利用天然微生物降解或改變有害物質成為無害或低毒性產物的方法,例如:利用植物來進行受金屬污染土地的復育工作、從輻射廢棄物中除去137Cs或從土壤中除去鎘等,這些相關技術目前均受到相當的關注。
參考資料:
1. Chelation。http://en.wikipedia.org/wiki/Chelation
2. Enterobactin。http://en.wikipedia.org/wiki/Enterobactin
3. Flo, T.H., Smith, K.D., Sato, A., Rodriguez, D. J., Holmes, M. A., Strong, R. K., Akira, S., & Aderem, A. Nature, 2004, 432, 917–921.
4. Metallothionein。http://en.wikipedia.org/wiki/Metallothionein
5. Phytochelatin。http://en.wikipedia.org/wiki/Phytochelatin
6. Siderophore。http://en.wikipedia.org/wiki/Siderophore
7. 利用生物技術進行土壤復育~應用基因轉殖植物吸收土壤重金屬。


 前一篇文章
前一篇文章 下一篇文章
下一篇文章 【2015諾貝爾化學獎特別報導】DNA修補─為生命提供化學的穩定
【2015諾貝爾化學獎特別報導】DNA修補─為生命提供化學的穩定  【2011諾貝爾化學獎】具有黃金比例的晶體
【2011諾貝爾化學獎】具有黃金比例的晶體  中間體與穩定狀態近似法
中間體與穩定狀態近似法  化學傳記:法拉第不為人知的一面(七):影響法拉第的宗教與人們
化學傳記:法拉第不為人知的一面(七):影響法拉第的宗教與人們 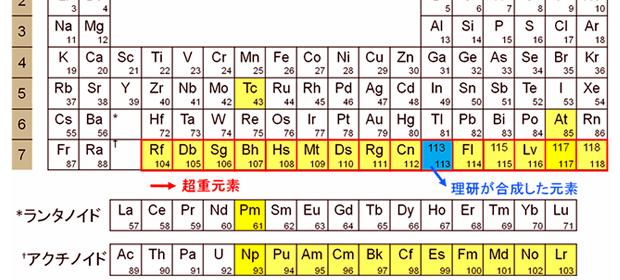 原子序第113超重元素的發現與命名
原子序第113超重元素的發現與命名  棉籽粕中殘留的棉籽酚
棉籽粕中殘留的棉籽酚 
