以實例說明如何繪製二成份系統的相圖(上)
以實例說明如何繪製二成份系統的相圖(上)
國立臺灣師範大學化學系兼任教師邱智宏
不論是純物質的相圖或是二成份混合物的相圖(binary phase diagram),其繪製方法均是依據真實的實驗數據加以呈現。但是基於對相圖本質上的了解,及實際的應用,若能在理想狀態下,根據熱力學的公式,利用實例練習如何繪製二成份混合物的相圖,將對相圖有更深入的理解及認知。
本文試以正庚烷(heptane)及正己烷(hexane)混合物的二成份系統,在固定溫度下,示範如何在定溫下製作壓力-成份相圖(pressure-composition phase diagram),並在(下)篇中說明如何在定壓下繪製溫度-成份相圖(temperature-composition phase diagram)。
首先,我們假設正庚烷及正己烷液體的混合為理想溶液,即各成份所呈現的蒸氣壓合乎拉午耳定律(Raoult’s law)。
$$p_A=X_Ap_A^*~~~~~~~~~(1)$$
其中 $$X_A$$ 為 $$A$$ 成份在溶液中所佔的莫耳分率,$$p_A^*$$ 及 $$p_A$$ 分別為 $$A$$ 成份的飽和蒸氣壓及分壓。正庚烷和正己烷在 $$70^\circ C$$ 時的飽和蒸氣壓分別為 $$767.6$$ 及 $$311.6~torr$$。
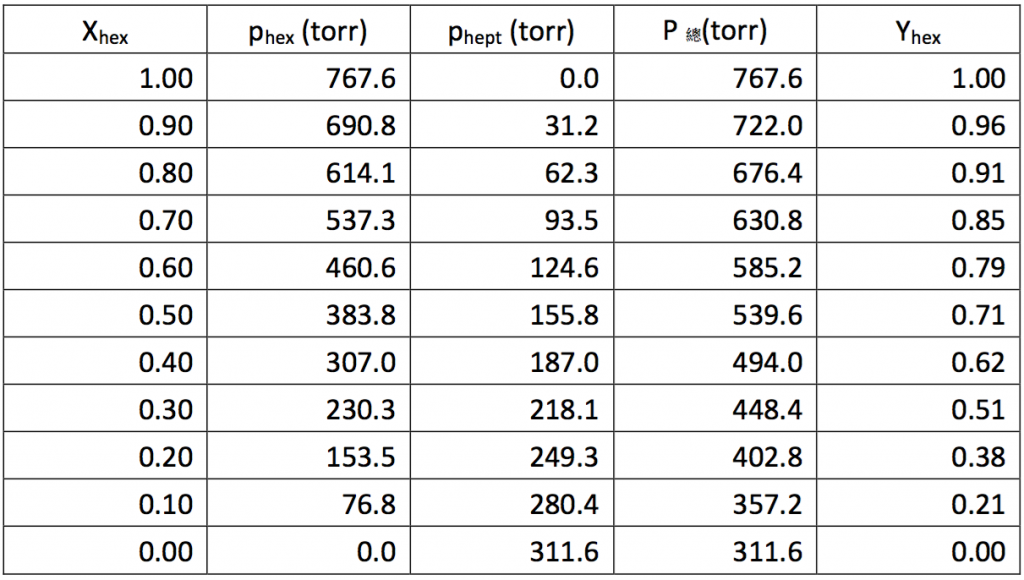
在不同莫耳分率時,根據式 $$(1)$$ 可算出二者分壓。若將兩者相加便可得到總壓(p總)。
p總 $$=p_{hex}+p_{hept}=X_{hex}p_{hex}^*+X_{hept}p_{hept}^*~~~~~~~~~(2)$$
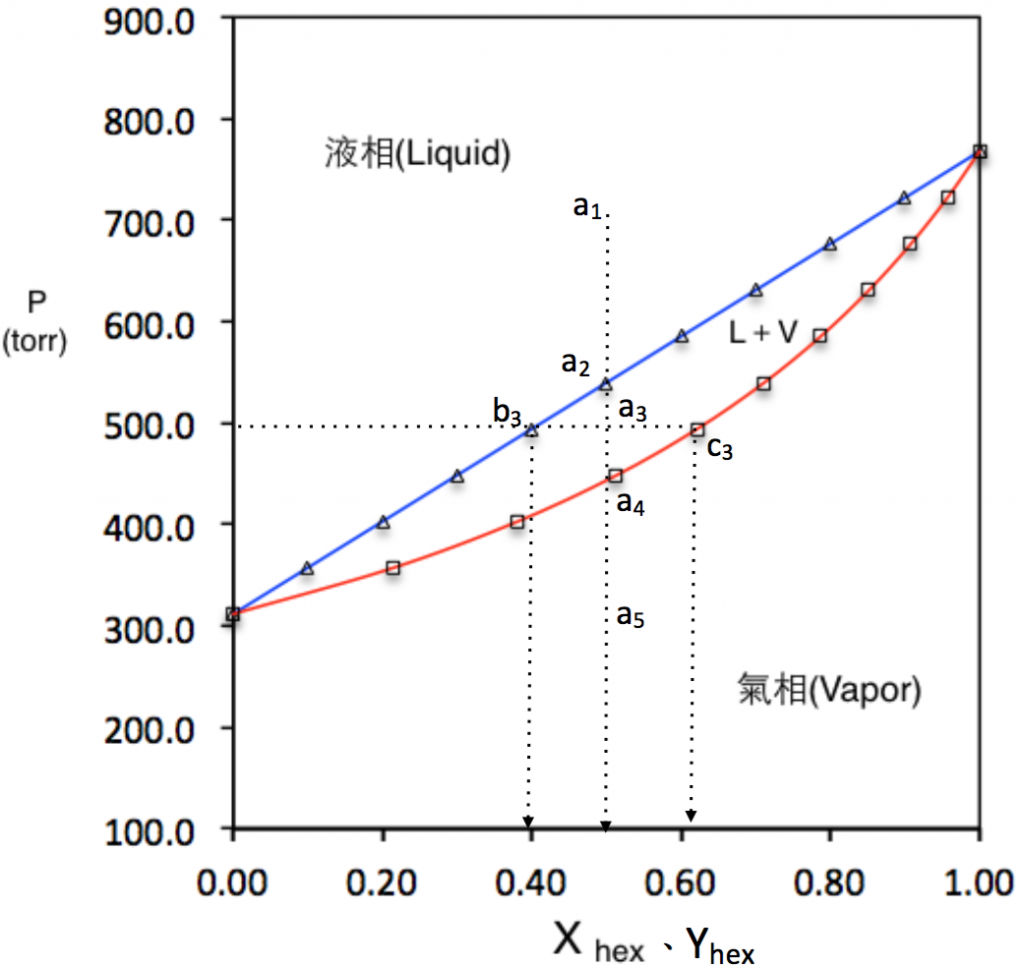
其中 $$p_{hex}$$、$$X_{hex}$$ 及 $$p_{hept}$$、$$X_{hept}$$ 分別為正己烷和正庚烷的分壓及莫耳分率,而且 $$X_{hex}+X_{hept}=1$$。將正己烷的莫耳分率由 $$0.1$$、$$0.2\cdots\cdots 1.0$$ 分別代入式 $$(2)$$,可得表一的結果。若將正己烷的莫耳分率對總壓作圖,則可得圖一中藍色的直線。
由上述的討論可知,液相中各成分的莫耳分率在配製時便已知曉,但是在氣相中各成份的莫耳分率各是多少呢?由於在氣相中的總壓及各分壓均已經拉午耳定律算出,所以其在氣相中的莫耳分率可表示如下:
$$Y_{hex}=p_{hex}/$$p總、$$Y_{hept}=1-Y_{hex}$$
其中 $$Y_{hex}$$、$$Y_{hept}$$ 分別代表氣相中正己烷、正庚烷的莫耳分率,將表一中第 $$2$$ 欄正己烷的分壓除以第 $$4$$ 欄的總壓,便能得到第 $$6$$ 欄的 $$Y_{hex}$$。若將總壓對氣相中正己烷的莫耳分率作圖,其結果如圖一中的紅色曲線。
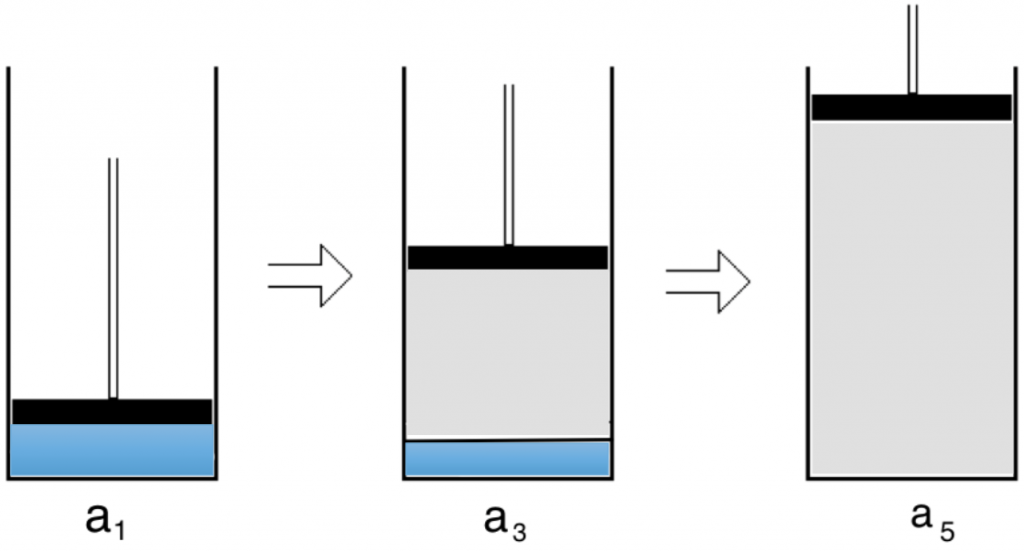
畫好相圖後,接下來探討如何解讀它。相圖中從 $$a_1$$、$$a_2\cdots\cdots$$到 $$a_5$$ 的變化過程,可以想像成將莫耳分率各為 $$0.5$$ 的正己烷及正庚烷裝入可調整壓力的容器中,如圖二所示。
在 $$a_1$$ 時容器內全為液體,隨著壓力減少,相當於圖二中的活塞往上拉,使體積變大。當相圖中的虚線碰到藍線的 $$a_2$$ 點時,開始有氣泡產生。若壓力再減至 $$a_3$$ 點時,此時氣相的含量更多,如圖二中間的圖示,此時氣、液相共存。由於 $$a_3$$ 點處有部分最初的液體氣化為氣相,此時正己烷在液相的莫耳分率,已經不再是 $$0.5$$,相同地氣相的莫耳分率也不是 $$0$$。此時通過 $$a_3$$ 點畫一條水平線,和藍、紅兩線分別交接於 $$b_3$$、$$c_3$$ 兩點,稱為連結線(tie line)。
回憶一下剛才的繪製過程,藍線交接點對應之橫座標為正己烷液相的莫耳分率,紅線交接點則為正己烷在氣相的莫耳分率,因此在 $$a_3$$ 點時,正己烷液相的莫耳分率為 $$0.4$$,而氣相的莫耳分率約為 $$0.62$$。若壓力再降至 $$a_4$$,開始所有液相均轉成氣相,從此以後没有液相,而氣相中各成份的莫耳分率則完全和最初 $$a_1$$ 點完全為液相時相同。
上述的所有繪製過程,均假設系統為理想溶液,如果是真實溶液則會產生偏差,圖形也會不太一樣,但是解讀相圖的方法則是不會改變。另外,壓力-成份相圖雖然容易繪製及說明,但是在實驗室及工業界中更常用的則是溫度-成份相圖,其繪製方式將在(下)篇中加以探究。
參考資料
- http://infohost.nmt.edu/~jaltig/LiqVapPhase.pdf
- P. W. Atkins, J. de Paula, “Physical Chemistry”, Oxford University Press, Oxford, 8th ed., p.179 (2006).


 前一篇文章
前一篇文章 下一篇文章
下一篇文章 強化玻璃
強化玻璃 ![[影音] CASE【百秒說科學】《交叉分子束》](https://highscope.ch.ntu.edu.tw/wordpress/wp-content/uploads/2016/11/CMB-620x280-科學Online.jpg) [影音] CASE【百秒說科學】《交叉分子束》
[影音] CASE【百秒說科學】《交叉分子束》  【2016年諾貝爾化學獎特別報導】如何將分子變成機器
【2016年諾貝爾化學獎特別報導】如何將分子變成機器  【2014諾貝爾化學獎】如何將光學顯微鏡變成奈米顯微鏡
【2014諾貝爾化學獎】如何將光學顯微鏡變成奈米顯微鏡  棉籽粕中殘留的棉籽酚
棉籽粕中殘留的棉籽酚 ![[新聞] 臺灣年輕團隊成功捕捉「克里奇中間體」與水分子的關鍵化學反應](https://highscope.ch.ntu.edu.tw/wordpress/wp-content/uploads/2015/01/221.jpg) [新聞] 臺灣年輕團隊成功捕捉「克里奇中間體」與水分子的關鍵化學反應
[新聞] 臺灣年輕團隊成功捕捉「克里奇中間體」與水分子的關鍵化學反應  油理油趣─淺談食油的化學
油理油趣─淺談食油的化學  目前世界上最精準的時鐘-光晶格光頻原子鐘在低溫環境下的突破
目前世界上最精準的時鐘-光晶格光頻原子鐘在低溫環境下的突破 
