3D有趣實驗:漂亮的綠色螢光(Beautiful Green Fluorescence)〔II〕
3D有趣實驗:漂亮的綠色螢光(Beautiful Green Fluorescence)〔II〕
國立彰化師範大學化學系學生李錡峰 / 國立彰化師範大學化學系楊水平副教授責任編輯
實驗影片
請按此連結,參閱「3D有趣實驗:漂亮的綠色螢光〔I〕」
原理和概念
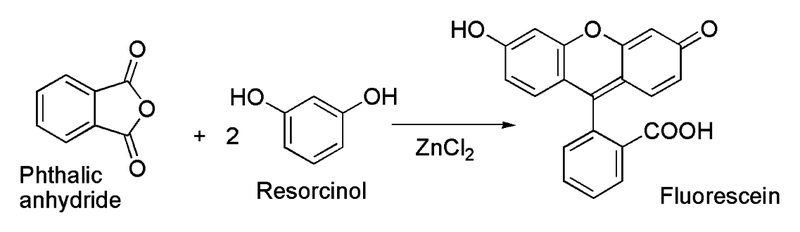
- 螢光素(Fluorescein)最早在1871年時由Adolf von Baeyer所製備出來,固體粉末為暗紅色,微溶於水但可溶於酒精,其實驗所使用Phthalic anhydride與Resorcinol來合成,其催化劑為氯化鋅,也可以使用硫酸作為催化劑,其反應式如下所示:
- 螢光是一種光致冷發光現象。當某種常溫物質經某種波長的入射光(通常是紫外線或X射線)照射,在吸收光能後,物質則進入激發態,並且立即回到基態並發出放射光(通常放射光的波長比入射光的波長為長,在可見光波段);而且一旦停止入射光,發光現象也隨之立即消失。具有這種性質的出射光就被稱之為螢光。
- 螢光素(Fluorescein)在水中的吸收波長最高約於494 nm,紫外光或一般的日光可以使螢光素躍升至激發態,而降到基態所放出的光的波長約於521 nm,是可見光範圍中的綠光,圖六為可見光各色光的波長光譜,由此圖可知綠色光譜的波長為495–570 nm。
- 螢光素(Fluorescein)的吸收度(absorbent)隨著溶液的pH值增大而增強(見圖七左圖),它的螢光放射(fluorescence emission)強度隨著溶液的pH值增大而增強(見圖七右圖)。再者,此物質的吸收波長隨著溶液的pH值增大而稍微增大(見圖七左圖),它的螢光放射波長隨著溶液的pH值增大而幾乎沒有改變(見圖七右圖)。
教學提示
- 本實驗使用濃硫酸且反應時會產生刺激性的黃色煙霧,建議在通風良好處或抽風櫃中進行實驗,並穿戴實驗衣、手套與安全眼鏡。
- 螢光素(Fluorescein)在太陽光或日光燈照射下也可觀察到綠色螢光,這是因為太陽光或日光燈有紫外光。建議使用高強度紫外光的UV燈在暗處檢驗,觀察螢光的效果較為顯著。
- 螢光素(Fluorescein)處於pH 9之環境,其螢光放射的強度較強,螢光素的螢光更容易觀察。
- 本實驗可改寫為教師示範,亦可改寫為實驗室實驗讓學生親自體驗合成螢光物質的樂趣。
問題與參考答案
- 螢光素(Fluorescein)是否需要特定波長的光的照射才能顯現其螢光?為什麼?
答:螢光素屬於螢光物質的一種,不同的螢光物質有不同的吸收波長,通常螢光物質需要特定光的照射,如紫外線、X射線等,才能顯現其螢光。 - 使用酞酐與間苯二酚合成螢光素(Fluorescein)時,停止加熱後是否必須停止攪拌?為什麼?
答:不能停止攪拌,若合成時停止攪拌,則會形成固體,因此必須繼續攪拌。 - 檢驗螢光素(Fluorescein)的螢光放射強度應該在酸性或中性或鹼性環境下為佳?為什麼?
答:應該在鹼性環境下為佳。這是因為此螢光物質的螢光放射(fluorescence emission)強度隨著溶液的pH值增大而增強
安全
- 操作本實驗應戴手套、穿實驗衣和戴安全眼鏡。
- 操作本實驗應該在通風良好之處或抽風櫃中操作,避免吸入刺激性的黃色煙霧。
- 實行適當的風險評估是老師的責任。
廢棄物處理
- 檢驗後的螢光液體應該倒入標示「有機物廢液桶」之桶中,集中處理。
參考資料
- SYNTHESIS OF FLUORESCEIN, a fluorescent dye, Christian A. Malapit, Organic Chemistry Laboratory, Department of Chemistry, Ateneo de Manila University.
- 螢光素,維基百科。
- Fluorescein, Wikipedia.
- 螢光,維基百科。
- Fluorescein, Oregon Green and Rhodamine Green Dyes—Section 1.5, Life Technologies.




 前一篇文章
前一篇文章 下一篇文章
下一篇文章![[講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講](https://highscope.ch.ntu.edu.tw/wordpress/wp-content/uploads/2015/10/Aaron-Ciechanover222.png) [講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講
[講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講  化學的填字遊戲?
化學的填字遊戲?  目前世界上最精準的時鐘-光晶格光頻原子鐘在低溫環境下的突破
目前世界上最精準的時鐘-光晶格光頻原子鐘在低溫環境下的突破  2014諾貝爾化學獎的遺珠:結構光照明顯微法
2014諾貝爾化學獎的遺珠:結構光照明顯微法 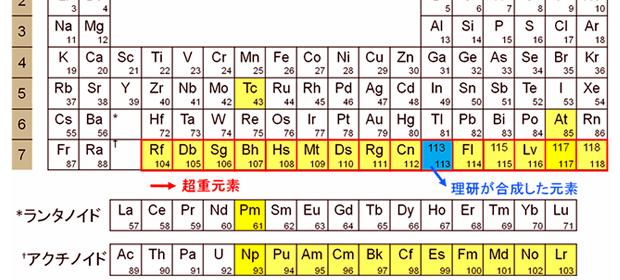 原子序第113超重元素的發現與命名
原子序第113超重元素的發現與命名  化學傳記:法拉第不為人知的一面(十一):凡人法拉第
化學傳記:法拉第不為人知的一面(十一):凡人法拉第  強化玻璃
強化玻璃 ![[新聞] 臺灣年輕團隊成功捕捉「克里奇中間體」與水分子的關鍵化學反應](https://highscope.ch.ntu.edu.tw/wordpress/wp-content/uploads/2015/01/221.jpg) [新聞] 臺灣年輕團隊成功捕捉「克里奇中間體」與水分子的關鍵化學反應
[新聞] 臺灣年輕團隊成功捕捉「克里奇中間體」與水分子的關鍵化學反應 
