沉澱(precipitation)
沉澱(precipitation)
台灣師範大學化學系葉名倉教授責任編輯
在化學領域中沉澱作用(precipitation)的過程是從反應的液相系統中產生一個可分離的固相,或是從過飽和溶液(supersaturation)中析出難溶性的固體。產生沉澱的化學反應又稱為沈澱反應(precipitation reaction)。以下列反應為例: 硝酸銀(AgNO3)水溶液與氯化鉀(KCl)水溶液混合可產生氯化銀(AgCl)沉澱及硝酸鉀(KNO3)水溶液,反應式表示方法為: AgNO3(aq) + KCl(aq)→ AgCl(s) + KNO3(aq)
此反應若以離子反應式表示,書寫如下: Ag+(aq) + NO3–(aq) + K+(aq) + Cl–(aq) → AgCl(solid) + K+(aq) + NO3–(aq)
刪除離子反應式中沒有發生沉澱反應的離子項目之後,
可得到淨離子反應式(net ionic reaction),書寫如下: Ag+(aq) +Cl–(aq)→ AgCl(solid)
物質的沉澱和溶解屬於化學平衡(equilibrium)的過程,計量的方法通常是用溶度積常數(solubility-product constant,Ksp)來判斷難溶鹽是否發生沉澱還是溶解。溶度積常數是指在一定溫度下,難溶性電解質的飽和溶液中,組成沉澱的各離子濃度的乘積為一常數。例如氯化銀的Ksp = 1.70×10-10,其值表示如下: Ag+(aq) +Cl–(aq)→ AgCl(s) Ksp = [Ag+“>[Cl–“>
沉澱可分為晶形沉澱和非晶形沉澱兩大類型。晶形沉澱內部排列較規則,結構緊密,可生長成較大顆粒,易於沉降和過濾;非晶形沉澱顆粒很小,沒有明顯的晶格,易形成膠質粒子(colloid),易吸附雜質,難以過濾。對非晶形沉澱,通常在熱、濃溶液中進行沉澱反應,同時加入大量電解質以加速沉澱微粒凝聚,防止形成膠體溶液。
沉澱過程的一個重要的起始階段是成核作用(nucleation)。成核作用的階段,要產生一個即將堅硬(hypothetical)的固體微粒需具備下列幾項條件:(1)在液體中先產生一個”液-固”界面(liquid-solid interface), 也就是在液體中的某處發生”液-固”相對的表面能量(surface energy)。如果沒有適當足量的表面能量,那麼就不會有成核作用的階段,溶液將形成過飽和溶液,而不會析出沉澱。
參考資料: http://encyclopedia.thefreedictionary.c … (chemistry)
http://encyclopedia.thefreedictionary.com/Solubility+product+constant
http://encyclopedia.thefreedictionary.com/colloid


 前一篇文章
前一篇文章 下一篇文章
下一篇文章 棉籽粕中殘留的棉籽酚
棉籽粕中殘留的棉籽酚  中間體與穩定狀態近似法
中間體與穩定狀態近似法  【2017年諾貝爾化學獎特別報導】將生命捕捉在原子的細節中
【2017年諾貝爾化學獎特別報導】將生命捕捉在原子的細節中 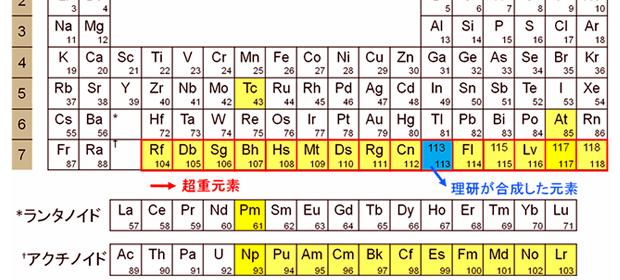 原子序第113超重元素的發現與命名
原子序第113超重元素的發現與命名  化學傳記:法拉第不為人知的一面(七):影響法拉第的宗教與人們
化學傳記:法拉第不為人知的一面(七):影響法拉第的宗教與人們 ![[講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講](https://highscope.ch.ntu.edu.tw/wordpress/wp-content/uploads/2015/10/Aaron-Ciechanover222.png) [講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講
[講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講  利用奈米粒子高效率吸收太陽能
利用奈米粒子高效率吸收太陽能 
