氯鹼工業(Chlor-alkali industry)
氯鹼工業(Chlor-alkali industry)
國立臺灣師範大學化學系大學部四年級陳昱勝
氯鹼工業(Chlor-alkali industry)顧名思義就是製備鹼與氯的方法。自從工業革命以後,酸與鹼在工業上的用途日益增大,由於化學工業發展的結果,酸與鹼更是化學工業的大宗。
在常溫下,氯氣是一種黃綠色、刺激性氣味、有毒的氣體,溶於水可生成鹽酸與次氯酸,並可進而製備過氯酸、氯酸、亞氯酸,皆為重要的工業原料。
氯氣得發現早在1774年由科學家卡爾•威廉•席勒(Carl Wilhelm Scheele)在實驗室裡利用鹽酸加上二氧化錳產生黃色氣體-氯氣。
HCl + MnO2 → MnCl2 + 2 H2O + Cl2
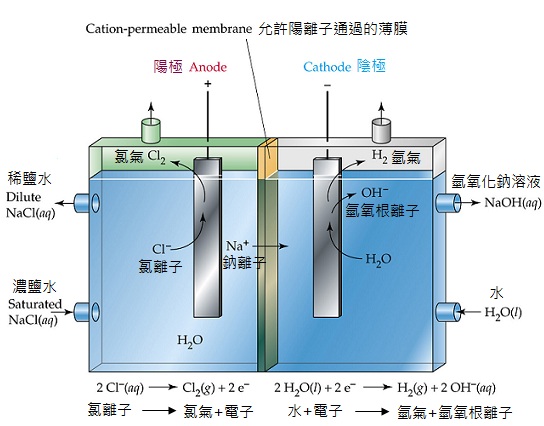
在工業上,氯氣常用電解食鹽水來生產製備,且可同時產生氫氣與氫氧化鈉,成為最有效率的製程方法。
2 NaCl + 2 H2O → Cl2 + H2 + 2 NaOH
利用電解方法,陽極發生氧化反應:
2 Cl– → Cl2 + 2 e–
陰極發生還原反應:
2 H2O + 2 e– → H2 + OH–
全反應為:2 NaCl + 2 H2O → Cl2 + H2 + 2 NaOH
而在兩電極中間隔有選擇性透膜,可讓陽離子通過以維持電中性,並且隔離氯氣與氫氣以避免兩氣體混和。加上飽和食鹽水與水的不斷提供,如此一來,可不斷地產生氫氣、氯氣、與氫氧化鈉水溶液,可謂將效率發揮的淋漓盡致。
除了利用食鹽製備氫氧化納、氯氣、氫氣之外,另一著名的鹼氯工業為製備碳酸鈉。碳酸鈉不論是在工業上與生活中都是最常使用的弱鹼、應用於玻璃、洗衣粉、氧化鋁製備、水的淨化軟化及洗滌等等。工業上常使用的有兩種方法,分別為路布蘭法(Leblanc process)與索爾維法(Solvay process)。
路布蘭法(Leblanc process):
1791年法國科學家尼古拉斯•勒布朗(Nicolas Leblanc)成功實現僅使用兩步驟即可從食鹽合成純的碳酸氫鈉的方法,由於步驟簡單,早期廣受業界使用:
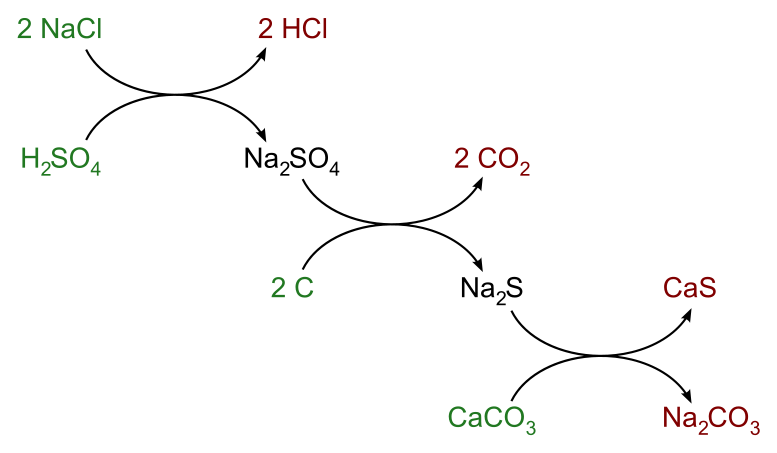
以食鹽、硫酸、煤粉、石灰石為原料,將食鹽與濃硫酸在800~900℃下混和,釋放出氯化氫氣體,同時得到硫酸鈉,再將硫酸鈉與煤粉和石灰石充分混和鍛燒而得碳酸鈉。副產物氯化氫為重要的工業原料、硫化鈣則可回收轉製成硫酸或硫酸銨。
其反應式為:
2 NaCl + H2SO4 → Na2SO4 + 2 HCl
Na2SO4 + CaCO3 + C → Na2CO3 + CaS +CO2
索爾維法(Solvay process):
1861年比利時化學家歐內斯特•索爾維(Ernest Solvay)發明了另之種製備碳酸鈉的方法,雖然其步驟複雜,但此方法消耗的原料少、成本低,成為到現今為止工業上最常使用的方法。
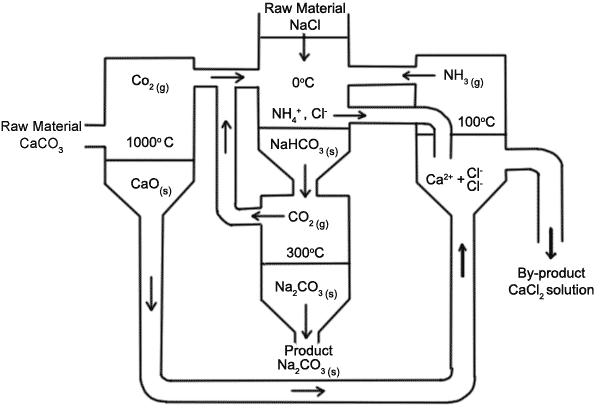
以食鹽、氨水、碳酸鈣為原料,碳酸鈣在高溫生成二氧化碳與氧化鈣,食鹽與二氧化碳和氨水反應生成碳酸氫鈉與氯化銨,碳酸氫鈉再加熱生成碳酸鈉、水、及二氧化碳,而生成的氯化銨可與氧化鈣反應生成氨水及氯化鈣。整個過程僅需持續提供碳酸鈣與食鹽,氨水與二氧化碳可循環再利用,即可持續產碳酸鈉與副產物氯化鈣。
其反應式為:
CaCO3 → CO2 + CaO
NaCl + CO2 + NH3 + H2O → NaHCO3 + NH4Cl
2 NH4Cl + CaO → 2 NH3 + CaCl2 + H2O
2 NaHCO3 → Na2CO3 + H2O + CO2
參考資料:
1. 路布蘭法http://en.wikipedia.org/wiki/Leblanc_process
2.電解食鹽水http://blog.udn.com/Gabriel33/6013067
3.氯鹼工業http://en.wikipedia.org/wiki/Chloralkali_process
4.碳酸鈉http://zh.wikipedia.org/zh-tw/%E7%A2%B3%E9%85%B8%E9%92%A0
5.索爾維法http://scifun.chem.wisc.edu/chemweek/Bicarb/SodiumBicarb.html


 前一篇文章
前一篇文章 下一篇文章
下一篇文章 【2015諾貝爾化學獎特別報導】DNA修補─為生命提供化學的穩定
【2015諾貝爾化學獎特別報導】DNA修補─為生命提供化學的穩定  化學傳記:法拉第不為人知的一面(五):兩個演講會
化學傳記:法拉第不為人知的一面(五):兩個演講會  【2017年諾貝爾化學獎特別報導】將生命捕捉在原子的細節中
【2017年諾貝爾化學獎特別報導】將生命捕捉在原子的細節中  【2014諾貝爾化學獎】如何將光學顯微鏡變成奈米顯微鏡
【2014諾貝爾化學獎】如何將光學顯微鏡變成奈米顯微鏡  謎樣的分子:克里奇中間體
謎樣的分子:克里奇中間體 ![[講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講](https://highscope.ch.ntu.edu.tw/wordpress/wp-content/uploads/2015/10/Aaron-Ciechanover222.png) [講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講
[講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講  化學的填字遊戲?
化學的填字遊戲? 
