盧奇還原反應
盧奇還原反應 (Luche Reduction)
國立臺灣師範大學化學系研究所 胡婷嘉
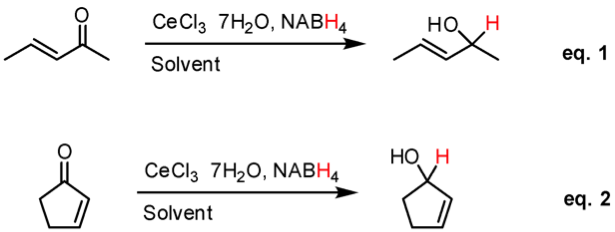
Luche 還原反應由 Jean Louis Luche 於 1978 年所提出,利用七水合三氯化鈰 $$\mathrm{(CeCl_3\cdot 7H_2O)}$$ 以及硼氫化鈉 $$\mathrm{(NaBH_4)}$$,以甲醇等醇類作為溶劑,將酮、醛以及 $$\alpha,\beta-$$不飽和醛酮有效且有選擇性的還原成烯醇類的方法(如 eq1、2)。
由於在加成的還原反應中,1, 2- 加成 (1, 2- addition) 和 1, 4- 加成 (1, 4- addition) 會彼此互相競爭,所以如何有選擇性的只走單一反應路徑還原酮或醛類化合物就變成很重要的問題了。在 Luche 反應中,主要得到 1, 2- 加成的還原產物,只有極少的 1, 4- 加成的副產物,是因為有硼氫化鈉的存在才有了選擇性。
以軟硬酸鹼理論 (Hard-Soft-Acid-Base, HSAB)。化學家們把酸和鹼分成硬和軟兩種,若一個粒子(原子、分子或離子)的半徑很小、帶的電荷很多,這些粒子就稱為硬酸 $$\mathrm{(H^+,Li^+,BF_3)}$$ 和硬鹼 $$\mathrm{(OH^-,RO^-,F^-)}$$,相反的,或若粒子半徑很大,電荷密度跟極性很小的話就稱為軟酸 $$\mathrm{(Hg^{2+},Ag^+,Au^+)}$$ 和軟鹼 $$\mathrm{(I^-,C_6H_6,SCN^-)}$$。
在其他條件相同時,硬酸和硬鹼會發生結合,反應較迅速,同時,軟酸和軟鹼也會有較快的反應速率。在 Luche 還原反應中,硼氫化鈉,半徑小而電荷密度大,為一個硬的鹼(此時為還原劑),所以會較傾向於攻打在不飽和酮中較硬的的羰基(此時為酸),而造成 1, 2-加成的結果。其反應機構如圖一。
首先,鈰離子先配位在甲醇的氧上面,和 $$\mathrm{^-BH_4}$$ 反應,脫掉一分子的氫氣形成 $$\mathrm{BH_3}$$、及甲氧基硼氫化鈉 $$(\mathrm{(BH_3\cdot OMe)Na})$$,重複以上步驟,最後形成帶有三個甲氧基的硼化物。
接著 $$(\mathrm{HB(OMe)_3Na,A})$$ 會攻打在 $$\alpha,\beta-$$不飽和酮的親電羰基上,因為三甲氧基硼氫化鈉是硬還原劑,所以較容易和羰基的地方進行反應,而且有三氯化鈰的存在會把羰基的碳氧雙見的電子拉向氧原子,使碳原子的電荷密度下降,利於三甲氧基硼氫化鈉的攻擊。
硼氫化鈉是最主要的還原劑,為氫的提供者,且在鈰離子的催化下形成硬的三甲氧基硼氫化鈉還原劑,使反應方向主要是進行 1, 2- 加成而不是 1, 4- 加成。
三氯化鈰 $$\mathrm{(CeCl_3)}$$ 先活化醇類的氧原子,使他的氫離子較易脫去,形成重要的三甲氧基硼氫化鈉還原劑,而且被活化的醇也會使要被還原的 $$\alpha,\beta-$$不飽和酮上的氧原子抓醇上的氫離子使碳氧雙鍵的電子向氧原子移動,使碳原子變成一個較易被還原劑攻打的位子。
在還原劑加了一個氫原子到羰基上之後,醇類的溶劑必須要提供一個氫原子給烷氧基,才會形成最後的產物。而且因為鈰原子催化的原因,會被活化,使硼氫化鈉成為三甲氧基硼氫化鈉之外,還可以活化羰基,使碳原子更容易被攻打。
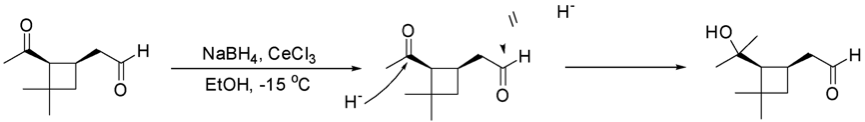
而且若在要被還原的分子中同時有醛和酮存在的時候,一般醛的反應性是比酮還要好的,所以會先還原醛基。但在 Luche 還原反應中,因為酮基的親電性比醛基還高,所以會先還原酮基,如圖二所示。
最後,此反應可以不影響化合物的羧酸、酯、酰胺、鹵化物、氰基和硝基等官能基,1, 2- 加成選擇性很好,產率高,速度快,可以在室溫下進行,不需排除空氣或水分,是一個操作很簡單的反應。
參考文獻
- The Luche reduction — University of Michigan, http://www.umich.edu/~chemh215/W09HTML/SSG3/ssg4/leading1.html
- References — University of Michigan, http://www.umich.edu/~chemh215/W09HTML/SSG3/ssg4/references.html
- Luche, J. L. (1978). Lanthanides in organic chemistry. 1. Selective 1, 2 reductions of conjugated ketones. Journal of the American Chemical Society, 100(7), 2226-2227.
- Conjugate Addition Reactions –, Chemwiki, http://chemwiki.ucdavis.edu/?title=Organic_Chemistry/Aldehydes_and_Ketones/Reactions_of_Aldehydes_%26_Ketones/Conjugate_Addition_Reactions
- Kurti, L., & Czakó, B. (2005). Strategic applications of named reactions in organic synthesis. Elsevier. pp. 268-269



 前一篇文章
前一篇文章 下一篇文章
下一篇文章 【2013諾貝爾獎特別報導】化學獎:將實驗帶入網際空間
【2013諾貝爾獎特別報導】化學獎:將實驗帶入網際空間  謎樣的分子:克里奇中間體
謎樣的分子:克里奇中間體  棉籽粕中殘留的棉籽酚
棉籽粕中殘留的棉籽酚  【2014諾貝爾化學獎】如何將光學顯微鏡變成奈米顯微鏡
【2014諾貝爾化學獎】如何將光學顯微鏡變成奈米顯微鏡  【2011諾貝爾化學獎】具有黃金比例的晶體
【2011諾貝爾化學獎】具有黃金比例的晶體  化學傳記:法拉第不為人知的一面(七):影響法拉第的宗教與人們
化學傳記:法拉第不為人知的一面(七):影響法拉第的宗教與人們  油理油趣─淺談食油的化學
油理油趣─淺談食油的化學 
