威廉遜醚類的合成法
威廉遜醚類的合成法(Williamson ether synthesis)
國立臺灣師範大學化學系碩士班二年級 鍾長志
亞歷山大.威廉.威廉遜 (Alexander William Williamson, 1824-1904)(圖一),出生於倫敦。
1844 年開始在吉森大學 Justus von Liebig 的實驗室工作。陸續在 1846 -1847 年間又發表了包含漂白鹽 (bleaching salts)、臭氧,以及普魯士藍 (Prussian blue) 等研究的期刊,其在化學史上有一重要的貢獻是威廉遜醚類的合成。2
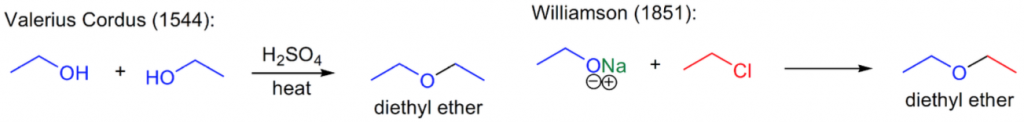
當時,因為已經有科學家發現硫酸和醇類反應會產生新的重排。威廉遜便設計了實驗,想藉由取代的方式製造出不同的醇類,再藉由不同的醇類合成醚類;在製造醇類的過程中,意外的發現了醚類可以透過乙醇鹽 (ethoxide) 和碘乙烷 (ethyl iodide) 製備。(圖二)
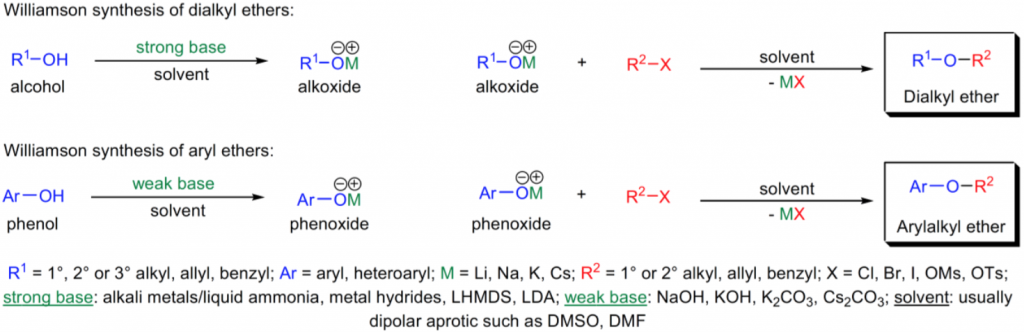
醚類的合成中,可以用醇類化合物或是酚類化合物作為起始物,加入強鹼反應得到烷氧化物 (alkoxide),接著與鹵烷化合物進行親核性反應得到醚類化合物(圖三)。
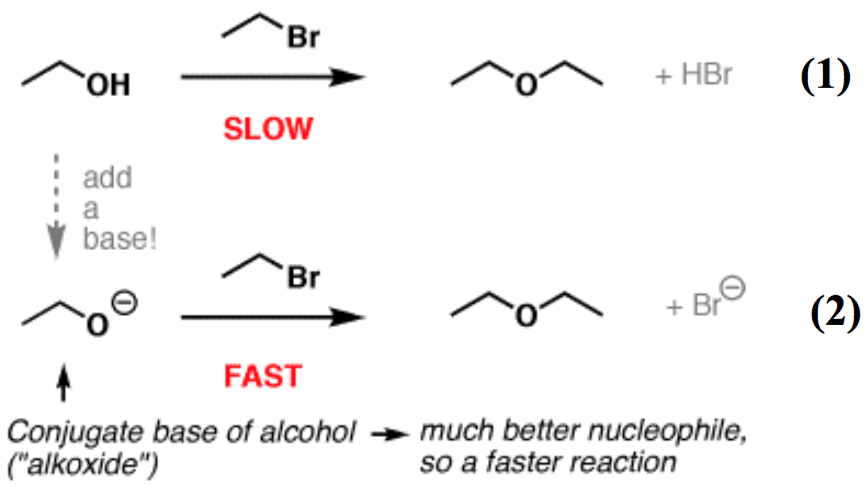
此反應需加入強鹼使得醇類變成醇鹽 (alcoholate),醇鹽上的氧電子雲密度較高,具有較好的親核性,如果沒有加入鹼會使得反應進行的很慢甚至無法反應。(圖四)
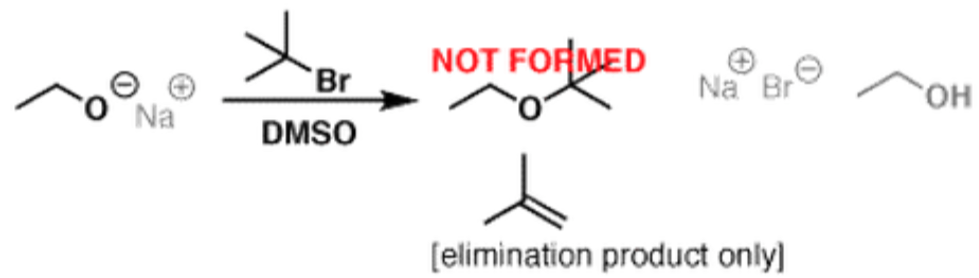
在威廉遜反應中,若如果選用的鹵烷類為三級鹵烷,因三級鹵烷的立體障礙過大無法進行取代反應,因此只會得到消去反應的產物 (elimination reaction)。(圖五)
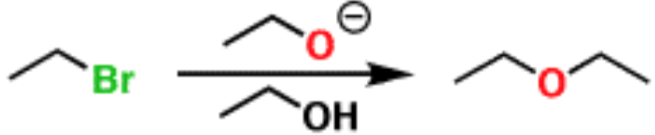
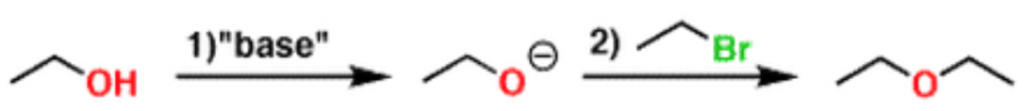
威廉遜反應最常見的方式就是如同圖六所示:將醇鹽類加入至烷基鹵化物,利用其共軛酸做為溶劑進行反應;此反應如圖七亦可從醇類開始,加入強鹼後、生成醇鹽,再加入烷基鹵化物。
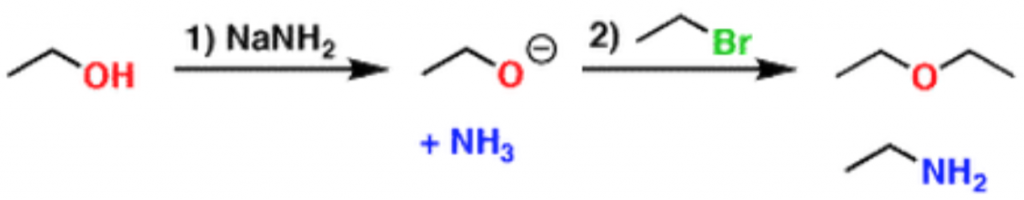
但,如果要對醇類進行去質子化,從酸鹼的角度來看,醇類的 $$pKa$$ 值約 $$16$$~$$18$$,而胺化鈉 $$\mathrm{({NH_2}^-Na^+)}$$ 的 $$pKa$$ 值約為 $$38$$,因此可做為鹼進行反應。
然而,反應中所產生會產生氨 $$(\mathrm{NH_3})$$ 也是一個很好的親核試劑 (nucleophile),會導致有非預期的副產物的生成,因此,胺化鈉對此反應來說並不是一個好的選擇(圖八)。
而若我們將強鹼物質改成氫化鈉 (sodium hydride),其 $$pKa$$ 值約 $$35$$,對醇類進行酸鹼反應亦是很好的強鹼,反應中所產生的氫氣不會進一步產生副反應,如圖九。由此例可知,在威廉森反應中鹼性物質的選擇也是一個重要的因素。
另外,在溶劑的選擇上也是一個相當重要的因素,見圖十。
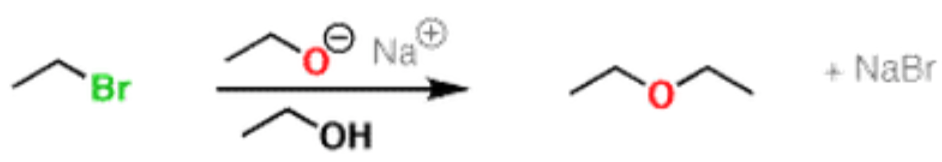
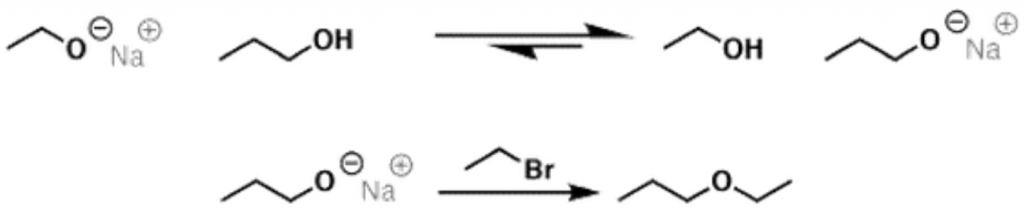
以圖十一舉例說明,威廉遜反應的溶劑必需為反應式中鹼性物質之共軛酸 (conjugated acid)。假設以丙醇作為溶劑,以乙醇鈉為此反應之鹼性物質,會有另一副反應的產生:乙醇鈉會和丙醇反應,產生丙醇鈉,此時氧帶負電荷、鈉帶正電荷;而氧帶負電荷具有很好的親核性,它也有可能與鹵烷進行反應,形成乙丙醚 (ethyl propyl ether) 這個非預期反應的副產物。
參考文獻
- Alexander William Williamson, http://www.goodreads.com/author/show/8131069.Alexander_William_Williamson
- Wisniak, J. (2009). Alexander William Williamson. Educación química, 20(3), 360-368
- Kurti, L., & Czakó, B. (2005).Strategic applications of named reactions in organic synthesis. Elsevier.
- The Williamson Ether Synthesis — Master Organic Chemistry. http://www.masterorganicchemistry.com/2014/10/24/the-williamson-ether-synthesis/
- Alkoxide — Wikipedia. http://en.wikipedia.org/wiki/Alkoxide



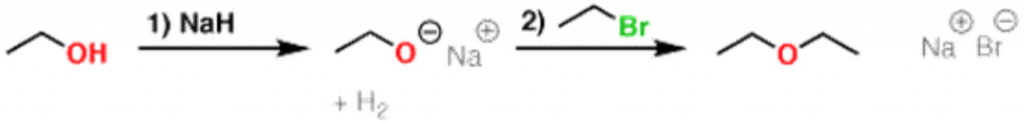
 前一篇文章
前一篇文章 下一篇文章
下一篇文章 化學傳記:法拉第不為人知的一面(二):從裝訂工變成大學者
化學傳記:法拉第不為人知的一面(二):從裝訂工變成大學者  【2014諾貝爾化學獎】如何將光學顯微鏡變成奈米顯微鏡
【2014諾貝爾化學獎】如何將光學顯微鏡變成奈米顯微鏡  利用奈米粒子高效率吸收太陽能
利用奈米粒子高效率吸收太陽能  不需溶劑的紅血球冷凍保存方法
不需溶劑的紅血球冷凍保存方法  油理油趣─淺談食油的化學
油理油趣─淺談食油的化學  中間體與穩定狀態近似法
中間體與穩定狀態近似法  暖暖包的原理
暖暖包的原理 
