克萊門森還原
克萊門森還原 (Clemmensen Reduction)
國立臺灣師範大學化學系碩士生 鍾長志
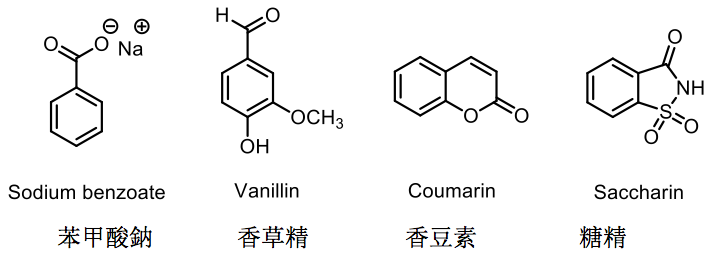
克萊門森 (Erik Christian Clemmensen),1876 年出生於丹麥,1900 年移居美國,之後開發克萊門森還原反應並且在 1913 年獲得哥本哈根大學博士學位。1914 年開始在製藥公司工作,分別開發了苯甲酸鈉 (sodium benzoate)、香草精 (Vanillin)、香豆素 (Coumarin) 的製造方法。他和友人創辦聯邦化工集團 (Commonwealth Chemical Corporation),後來被孟山都化學公司 (Monsanto Company) 併購,並且與合作夥伴開發出糖精 (Saccharin)。克萊門森於 1941 年逝世,本文所要介紹的克萊門森還原是其最著名的代表作1。
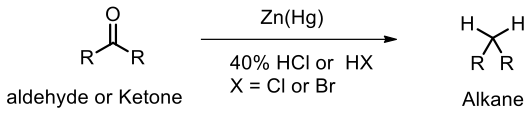
克萊門森還原於 1913 年發表,此方法廣泛應用在醛類化合物及酮類化合物的還原,主要是利用鋅汞合金以及鹽酸將醛和酮的羰基上之氧原子還原成兩個氫原子。此反應的應用性很廣,也包括了芳香族化合物,另外在複雜天然物的合成中,此反應更是經常被使用的合成策略。2
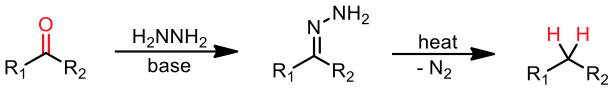
這個方法是將羰基還原成碳氫化合物 (hydrocarbons),很多種還原試劑會把醛或酮還原成醇類化合物。此外,沃夫-奇希諾還原 (Wolff-Kishner reduction)3 和克萊門森還原也有著異曲同工之妙,前者是利用肼 (hydrazine) 和鹼 (alkali),將醛類或酮類還原成碳氫化合物。
克萊門森還原反應機制5-7 並沒有一個真正的答案,大致上可分為兩派:一派則是以類碳烯為反應機構之主架構 (Carbenoid mechanis),以自由基的形式在鋅金屬表面進行還原反應4;另一派是以碳陰離子為反應機構之主架構 (Carbanionic mechanism),主要認為鋅會直接攻擊在被質子化的羰基上4。
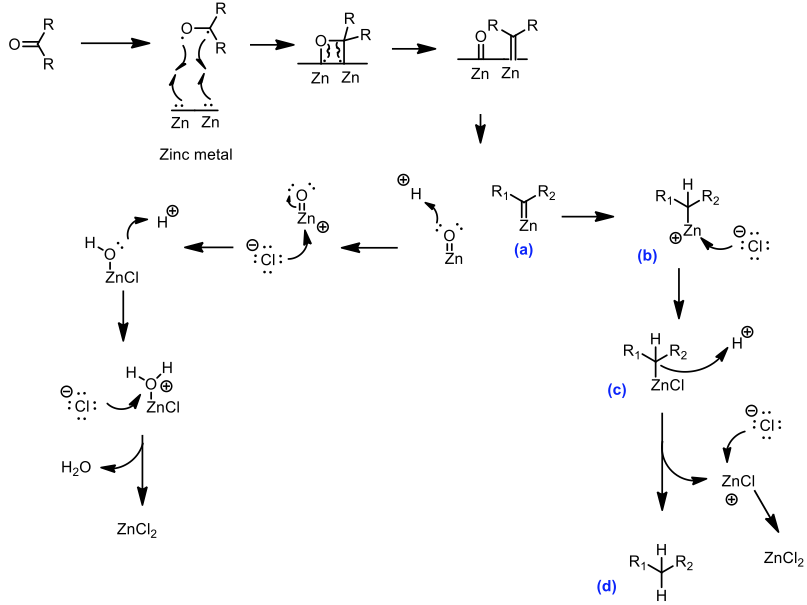
類碳烯反應機制如圖五所示:一開始,醛或酮類等羰基化合物透過鋅金屬的活化,以電子轉移的方式與鋅金屬形成中間體,形成鋅類碳烯 (zinc carbenoid, (a)),氫接著打在與化合物 (b) 中與鋅鍵結的碳上,氯負離子再攻打至鋅金屬上得到中間體 (c),從電負度的觀點判斷,在碳鋅鍵的電子雲密度的分布應是較靠近碳的,且碳與金屬鋅的鍵結相較於碳與氫的鍵結是比較弱的,因此中間體 (c) 的碳便可以用碳陰離子的形式存在,使之更易與陽離子鍵結,與氫離子鍵結後就完成了還原反應得最終產物 (d)。
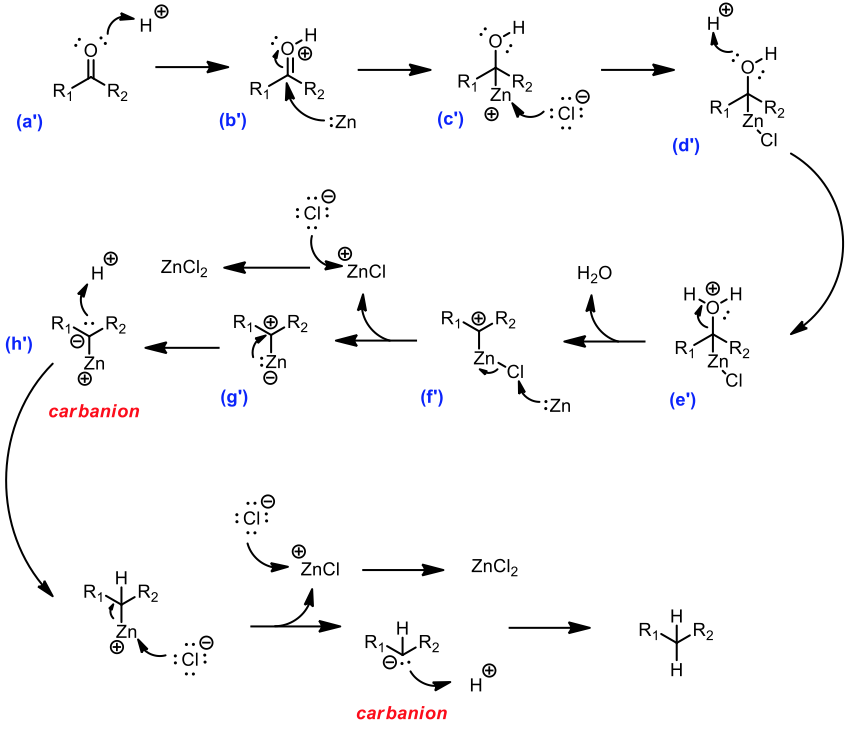
碳陰離子反應機制如圖六所示:首先鹽酸提供氫離子,對化合物 (a’) 羰基進行質子化,得到 (b’),此時氧原子比較偏正電荷,又因電子效應的關係,氧的電負度比碳大,使得碳可用碳陽離子的形態存在,因此鋅(汞)合金容易提供電子對給碳形成醇類得到 (c’),氯負離子在與鋅金屬鍵結,使形成較穩定存在的 (d’)。醇上的氧再進行質子化形成中間體 (e’),此時氧帶正電為一好的離去基,可以脫去水,形成具碳陽離子結構的中間體 (f’),此中間體是較不穩定的結構,因此另外一個鋅與氯作用 (g’),能使得鋅能夠提供電子給碳陽離子並穩定此碳陰離子中間體 (h’),(h’) 再與一氫離子鍵結、再重複步驟即可得到還原後的產物4。
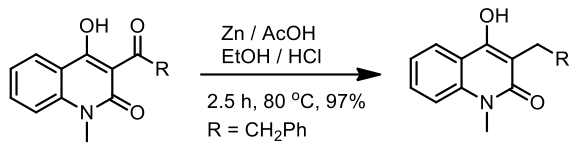
克萊門森還原在條件上非常嚴苛,以 40% 鹽酸水溶液及鋅汞合金為條件,且以疏水性的有機溶劑作為溶劑,例如甲苯。在一些對酸比較敏感的化合物及較多官能基的化合物中沒有辦法達到比較好的效果。Yamamura 教授和他的夥伴利用加入其他有機溶劑 (THF, Et2O, Ac2O) 與鹵化氫 (hydrogen halide) 及活化過的鋅粉反應,此方法可以幫助反應物的溶解度增加(因很多羰基化合物在甲苯溶劑中溶解度較差)進而增加反應性8,如圖七。
參考文獻
- Erik Christian Clemmensen — http://www.snipview.com/q/Erik_Christian_Clemmensen
- Surrey, A. (1961). Name Reactions in Organic Chemistry. Elsevier Science.
- Wolff–Kishner reduction — http://en.wikipedia.org/wiki/Wolff%E2%80%93Kishner_reduction
- Clemmensen reduction — Name-Reaction.com. http://www.name-reaction.com/clemmensen-reduction
- Clemmensen Reduction — UC Davis ChemWiki. http://chemwiki.ucdavis.edu/?title=Organic_Chemistry/Aldehydes_and_Ketones/Reactions_of_Aldehydes_%26_Ketones/Clemmensen_Reduction
- Clemmensen Reduction of Carbonyl compounds —https://www.youtube.com/watch?v=PESoEqyJHRU
- Clemmensen Reduction — http://www.synarchive.com/named-reactions/Clemmensen_Reduction
- Kurti, L., & Czakó, B. (2005). Strategic applications of named reactions in organic synthesis.
- Kappe, T., Aigner, R., Roschger, P., Schnell, B., & Stadibauer, W. (1995). A simple and effective method for the reduction of acyl substituted heterocyclic 1, 3-dicarbonyl compounds to alkyl derivatives by zinc-acetic acid-hydrochloric acid. Tetrahedron, 51(47), 12923-12928.



 前一篇文章
前一篇文章 下一篇文章
下一篇文章 化學傳記:法拉第不為人知的一面(六):電磁轉動與電磁感應
化學傳記:法拉第不為人知的一面(六):電磁轉動與電磁感應  棉籽粕中殘留的棉籽酚
棉籽粕中殘留的棉籽酚  謎樣的分子:克里奇中間體
謎樣的分子:克里奇中間體 ![[講義] 科學史沙龍:陳竹亭教授、楊信男教授](https://highscope.ch.ntu.edu.tw/wordpress/wp-content/uploads/2015/01/科學史.png) [講義] 科學史沙龍:陳竹亭教授、楊信男教授
[講義] 科學史沙龍:陳竹亭教授、楊信男教授  2014諾貝爾化學獎的遺珠:結構光照明顯微法
2014諾貝爾化學獎的遺珠:結構光照明顯微法  【2014諾貝爾化學獎】如何將光學顯微鏡變成奈米顯微鏡
【2014諾貝爾化學獎】如何將光學顯微鏡變成奈米顯微鏡 
