根岸交叉耦合反應
根岸交叉耦合反應(Negishi Cross-coupling Reaction)
國立臺灣師範大學化學系博士生 林欣慧
背景介紹
本反應是由根岸英一(Ei-ichi Negishi,圖一)1 教授於 1976 年發表。根岸教授生涯致力於有機金屬的研究,因成功針對使用鎳或鈀催化的有機鹵烴 (organic halide) 交叉耦合反應進行改善,於 2010 年與鈴木章 (Suzuki Akira)、理察.赫克 (Richard Heck) 三人共同獲頒諾貝爾化學獎。此外,根岸教授所發表的研究成果亦有許多已成功應用在工業合成,本文將要介紹的反應也是其中之一。3,4
有機化合物中最重要的部分非屬碳—碳鍵結莫屬,因此有機化學家皆致力於研究 C–C 鍵結方法的開發。1972 年熊田誠 (Makoto Kumada) 教授及其研究團隊率先發表利用鎳或鈀催化格里納試劑 (Grinard reagent) 與有機鹵烴進行交叉耦合反應3(即熊田交叉耦合反應,Kumada cross-coupling,圖二)。
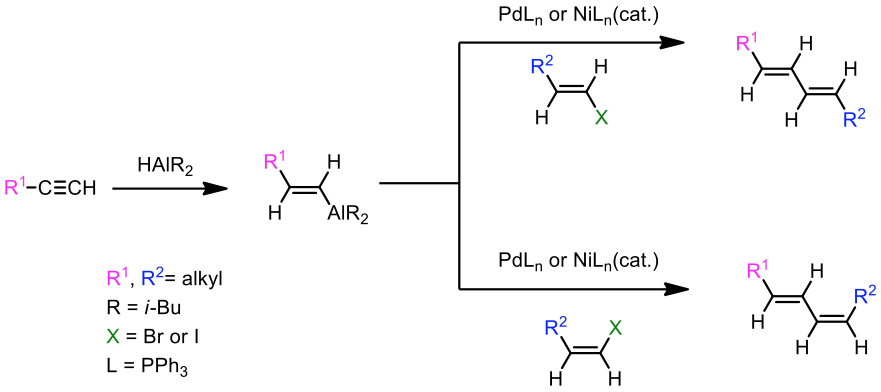
雖然此反應可形成有機化合物中最重要的 C–C 鍵結,可惜鋰或鎂的金屬性太強導致於反應物的官能基選擇受限,於是此反應的改良便成為當代的研究重點之一,尋找一種金屬性較鋰或鎂金屬弱的有機金屬試劑,藉此提高反應物官能基對所選用的有機金屬試劑容忍度便成為重要的目標。1976 年,根岸教授及其團隊發表了首篇利用有機鋁試劑 (organoaluminums) 與有機鹵烴在鎳或鈀的催化下進行交叉耦合反應4,如圖三所示。
根岸交叉耦合反應3 最重要的地方不僅在其大大地拓展了反應物官能基的選擇度,更在於它相當地具有立體專一性 (stereospecificity)。事實上,根岸教授最初提出時是使用有機鋁試劑來與有機鹵烴進行交叉耦合,然而有機鋁試劑雖然能夠提升官能基的選用範圍,但使用鎳做為催化劑時,可看到有機鋁試劑的自耦合 (homocoupled) 產物生成,無法達到理想的立體專一性。因此進一步的改良後發現,使用有機鋅試劑 (organoznic reagents) 的話,鎳和鈀皆能進行催化,但鈀試劑無論在反應速率、產率、立體選擇性甚至是反應物官能基的多變性表現上,皆較鎳試劑優秀,如圖四所示。
鎳試劑催化的反應機構
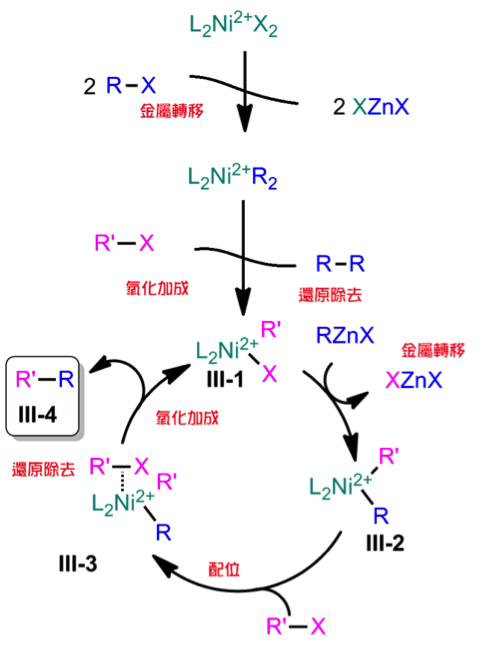
首先,有機鎳試劑會先與有機鋅試劑進行金屬轉移 (transmetallation),接著有機鹵烴會參與進來並進行氧化加成 (oxidative addition) 後得到的中間體 III-1;再來此中間體會和有機鋅試劑再進行金屬轉移後得到中間體 III-2 並與有機鹵烴進行配位後得到配位錯合物 III-3,最後再進行還原除去 (reductive elimination) 可得到我們所預期進行交叉耦合反應後的產物 R’–R (III-4)。
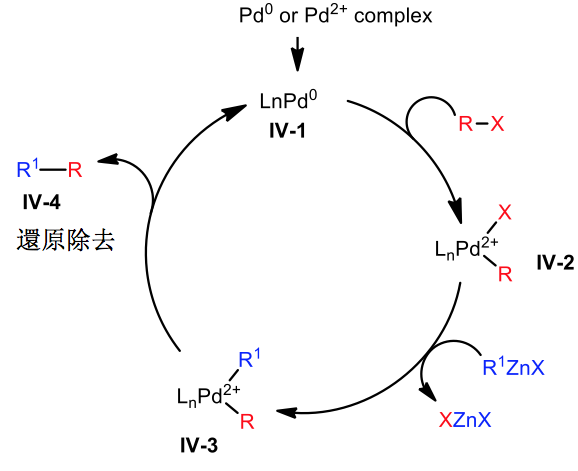
鈀試劑催化的反應機構
與鎳催化相似,首先鈀試劑 IV-1 先與有機鹵烴進行氧化加成形成錯合物 IV-2;接著與有機鋅試劑進行金屬轉移後形成中間體 IV-3,最後經過還原除去的步驟即可得到進行交叉耦合反應後的產物 R’–R (IV-4)。
實際應用
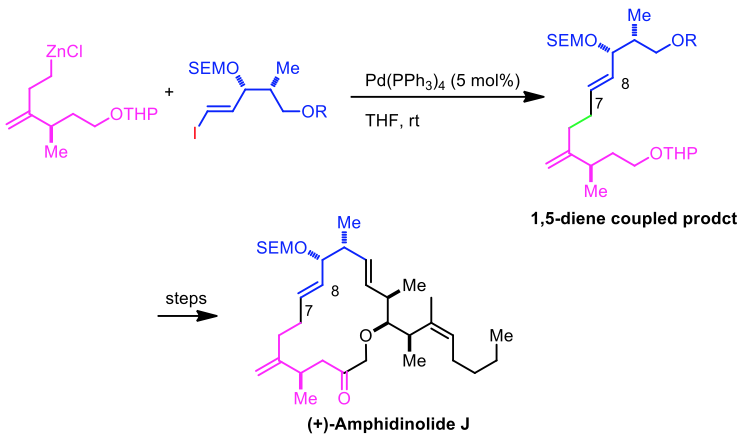
1998 年 Williams 教授及其研究團隊發表於期刊 J. Am. Chem. Soc.:如何合成巨環分子 (+)-Amphidinolide J。5 我們從圖五中可以發現該巨環分子中具有一個關鍵的反式雙鍵(7 號碳及 8 號碳的位置),而作者便是利用根岸交叉耦合反應所具備的良好立體專一性進行該雙鍵的合成。首先,作者先在反應瓶中進行所需的有機鋅試劑製備;接著在鈀試劑的催化下與一個具有反式雙鍵的鹵烯分子進行根岸交叉耦合反應便可得到具有反式雙鍵的耦合產物。最後再進行後續的合成步驟即可得到作者所預期的巨環分子 (+)-Amphidinolide J。
結論
根岸交叉耦合反應有以下幾個特點:
- 此反應成功地找到一個有機金屬試劑以增加反應物的官能基容忍度。
- 此反應可利用鎳及鈀進行催化,然而使用鈀進行催化的效果較鎳為佳。
- 此反應具有良好的立體專一性。
- 雖然催化所需的鎳(0) 及鈀(0) 錯合物較不穩定,但可利用較為穩定的鎳2+ 及鈀2+ 錯合物並添加還原劑以產生所需的催化劑。
參考文獻
- 根岸英一|維基百科。https://zh.wikipedia.org/wiki/%E6%A0%B9%E5%B2%B8%E8%8B%B1%E4%B8%80
- Ei-ichi Negishi – Biographical — Nobelprize.org. http://www.nobelprize.org/nobel_prizes/chemistry/laureates/2010/negishi-bio.html
- Kürti, L. & Czakó, B. (2005). Strategic applications of named reactions in organic synthesis. Amsterdam: Elsevier Academic Press.
- Baba, S., & Negishi, E. (1976). A novel stereospecific alkenyl-alkenyl cross-coupling by a palladium-or nickel-catalyzed reaction of alkenylalanes with alkenyl halides. Journal of the American Chemical Society, 98(21), 6729-6731.
- Williams, D. & Kissel, W. (1998). Total Synthesis of (+)-Amphidinolide J. J. Am. Chem. Soc., 120(43), 11198-11199. http://dx.doi.org/10.1021/ja982572d



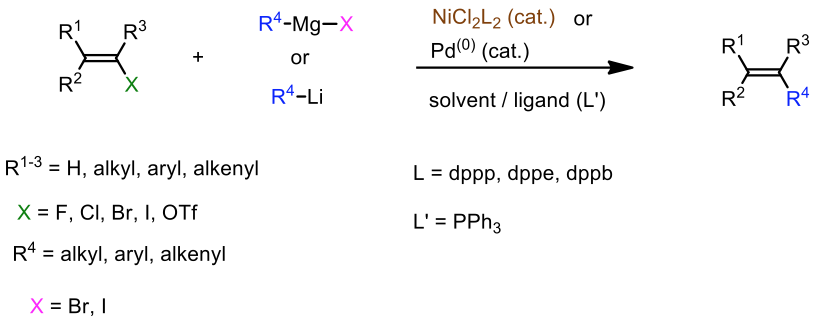
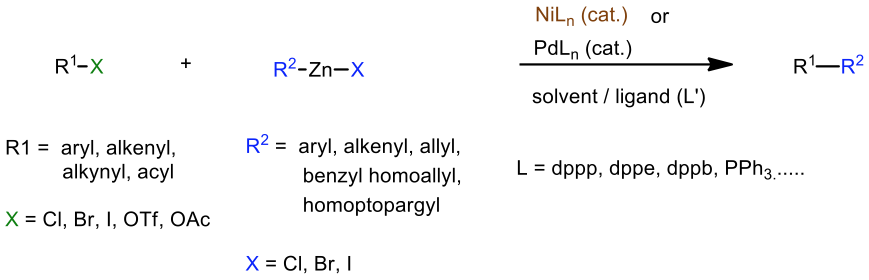
 前一篇文章
前一篇文章 下一篇文章
下一篇文章 化學傳記:法拉第不為人知的一面(十一):凡人法拉第
化學傳記:法拉第不為人知的一面(十一):凡人法拉第  【2011諾貝爾化學獎】具有黃金比例的晶體
【2011諾貝爾化學獎】具有黃金比例的晶體 ![[講義] 科學史沙龍:陳竹亭教授、楊信男教授](https://highscope.ch.ntu.edu.tw/wordpress/wp-content/uploads/2015/01/科學史.png) [講義] 科學史沙龍:陳竹亭教授、楊信男教授
[講義] 科學史沙龍:陳竹亭教授、楊信男教授  【2019諾貝爾化學獎】鋰離子電池
【2019諾貝爾化學獎】鋰離子電池  謎樣的分子:克里奇中間體
謎樣的分子:克里奇中間體  【2013諾貝爾獎特別報導】化學獎:將實驗帶入網際空間
【2013諾貝爾獎特別報導】化學獎:將實驗帶入網際空間 
