化學實驗室實驗:氫氣與氯氣的光化學反應(Photochemical Reactions of Chlorine with Hydrogen)〔I〕
化學實驗室實驗:氫氣與氯氣的光化學反應(Photochemical Reactions of Chlorine with Hydrogen)〔I〕
國立彰化女子高級中學化學科張文平老師 / 國立彰化師範大學化學系楊水平副教授責任編輯
學生講義之一(Student Handout I)
實驗介紹
本實驗的目的是以注射筒進行氫氣與氯氣的微量製備,並利用燃燒鎂帶產生紫外光當作光化學反應的光源,照射裝在注射筒中的氫氣與氯氣之混合氣體,觀察反應的變化情形並檢驗反應後產生氣體的性質。
氫氣和氯氣在室溫下並不發生反應,就像氫氣和氧氣一樣。然而,若氫氣在空氣中被點燃,則會達到活化能而發生快速反應並產生火焰。由於此反應為放熱反應,因 此溫度急速上升,局部區域的氣體快速膨脹,而造成爆炸。若在紫外光的照射下,則氫氣和氯氣也可以達到活化能而發生光化學反應,如反應式[1]所示:
H2(g) + Cl2(g) → 2HCl(g) [1]
紫外光加速氫氣和氯氣的光化學反應是自由基的鏈鎖反應,起始步驟是氯分子吸收紫外光,導致Cl-Cl鍵斷裂,而形成氯原子自由基,每個氯原子有一個未成對電子,如反應式[2]所示。
Cl2(g) → Cl•(g) + Cl•(g) [2]
Cl-Cl的鍵能有243千焦/莫耳,其能量相當於波長約500 nm,亦即在藍綠區域的可見光區,此鍵能可以被紫外光打斷。
在紫外光下,氫氣與氯氣的鏈鎖反應之反應機構,如反應式[2]~[4]所示:
Cl2(g) → Cl•(g) + Cl•(g) [2] Cl•(g) + H2(g) → HCl(g) + H•(g) [3] H•(g) + Cl2(g) → HCl(g) + Cl•(g) [4]
氫氣與氯氣的結束鏈鎖反應,如反應式[5]~[9]所示:
2Cl•(g) → Cl2(g) [5] 2H•(g) → H2(g) [6] H•(g) + Cl•(g) → HCl(g) [7] H•(g) + O2(g) → HO2•(g) (含有空氣時) [8] Cl•(g) + O2(g) → ClO2•(g) (含有空氣時) [9]
雖然在整體的光反應中,反應物(氫氣和氯氣)與產物(氯化氫)的莫耳數變化並沒有增減,但是由於此反應為放熱(93 kJ/mol HCl)反應,因此導致產物氣體和混合氣體的溫度快速上身而造成膨漲,使得注射針橡皮塞向外噴出。
氫氣與氯氣反應產生的產物為氯化氫氣體,若氯化氫氣體與氨氣混合,則有白色煙霧產生,因此可以用氨氣來檢驗氯化氫氣體,其反應如反應式[10]所示。
HCl(g) + NH3(g) → NH4Cl(s) [10]
藥品和器材
1. 注射筒(容量50 mL)並附注射筒橡皮塞 3個/組
2. 剪刀(小支) 1支/組
3. 燒杯(100 mL) 3個/組
4. 直尺 1支/組
5. 量筒(10 mL) 1支/組
6. PE滴管(3 mL) 1支/組
7. 電子天平(0.01 g或更精確) 2台/班
8. 保特瓶(1000 mL) 1個/組
9. 護目鏡 1副/組
10. 鐵架及鐵夾 1組/組
11. 乳膠手套 1副/組
12. 鎂帶(Magnesium, Mg) 5 cm/組
13. 鎂帶(Magnesium, Mg) 10 cm/組
14. 打火機 1個/組
15. 太陽眼鏡 1副/組
16. 耳塞 1副/組
17. 3% 次氯酸鈉溶液(sodium hypochlorite, NaOCl, solution) 10 mL/組
18. 1.0 M鹽酸(Hydrochloric acid, HCl(aq)) 100 mL/組
19. 濃氨水(Conc. ammonia water, NH3(aq)) 5 mL/組
實驗步驟
A:氫氣的製備
1. 用剪刀取約5公分(約0.050克)的鎂帶,備用。
2. 取一個注射筒橡皮塞緊密地套住一支塑膠注射筒(編號A)的前端出口處,並在注射筒內裝約20 mL的自來水,如圖一所示。
3. 放置步驟1的鎂帶於注射針筒內,使其沉於底部,如圖二所示。
4. 插入針筒推桿(活塞)到注射筒內,先手持注射筒使開口朝上,取下注射筒橡皮塞,推進針筒推桿,以排除空氣。然後放置於一個保特瓶的瓶口,推進針筒推桿,以排除大部分的水,避免殘留空氣,如圖三所示。
5. 拉起注射筒的針筒推桿,吸取約20 mL的1.0 M HCl,如圖四所示,並迅速套住橡皮塞。此時開始發生反應而產生氣泡,立即手持注射筒橡皮塞朝下並壓住桌面,使之緊密連接在一起,以避免氣體從注射筒的開口處逸出。隨後反應快速發生,針筒推桿會往外推開。
6. 在反應完全後,卸下橡皮塞。放置此注射筒於一個保特瓶的瓶口上,排除未反應的稀鹽酸,保留氫氣在注射筒中,如圖五所示。
7. 在完全排除未反應的稀鹽酸後,套上注射筒橡皮塞,收集約30 mL的氫氣備用,如圖六所示。
B:氯氣的製備
1. 取另一支注射筒(編號B),先在開口前端處連接一小段的橡皮管,於橡皮管的一端套上橡皮塞。然後倒入約20 mL的自來水到注射筒內,如圖七所示。
2. 插入針筒推桿(活塞)到注射筒內,先手持注射筒使開口朝上,取下注射筒橡皮塞,推進針筒推桿,以排除空氣。然後放置於一個保特瓶的瓶口,推進針筒推桿,以排除大部分的水,避免殘留空氣,如圖八所示。
3. 手戴乳膠手套,以避免接觸次氯酸鈉漂白水(NaOCl溶液)。先吸取約5.0 mL的3%次氯酸鈉漂白水,如圖九所示。
4. 再吸取約20 mL的1.0 M HCl,如圖十所示。套上注射筒橡皮塞,此時開始發生反應而產生氣泡,立即手持注射筒橡皮塞朝下並壓住桌面,使之緊密連接在一起,以避免氣體從注射筒的開口處逸出。隨後反應快速發生,針筒推桿會往外推開。
5. 在反應完全後,卸下注射筒橡皮塞。放置此注射筒於保特瓶瓶口上,排除未反應的稀鹽酸,保留氯氣在注射筒中,如圖十一所示。
6. 在完全排除未反應的稀鹽酸後,套上注射筒橡皮塞,收集約30 mL的氯氣備用,如圖十二所示。














 前一篇文章
前一篇文章 下一篇文章
下一篇文章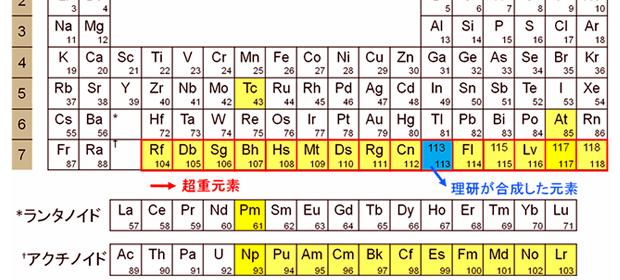 原子序第113超重元素的發現與命名
原子序第113超重元素的發現與命名  利用奈米粒子高效率吸收太陽能
利用奈米粒子高效率吸收太陽能  化學傳記:法拉第不為人知的一面(八):電解定律
化學傳記:法拉第不為人知的一面(八):電解定律 ![[講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講](https://highscope.ch.ntu.edu.tw/wordpress/wp-content/uploads/2015/10/Aaron-Ciechanover222.png) [講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講
[講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講  【2017年諾貝爾化學獎特別報導】將生命捕捉在原子的細節中
【2017年諾貝爾化學獎特別報導】將生命捕捉在原子的細節中  【2011諾貝爾化學獎】具有黃金比例的晶體
【2011諾貝爾化學獎】具有黃金比例的晶體  【2014諾貝爾化學獎深入報導】 打破光學顯微鏡的解析度極限-超高解析螢光顯微法
【2014諾貝爾化學獎深入報導】 打破光學顯微鏡的解析度極限-超高解析螢光顯微法 
