化學傳記:1902年諾貝爾化學獎得主-費雪(Hermann Emil Fischer)(二)
化學傳記:1902年諾貝爾化學獎得主-費雪(Hermann Emil Fischer)(二)
國立臺灣師範大學化學系江宣儀碩士生/國立台灣師範大學化學系葉名倉教授責任編輯

以費雪命名的重要化學貢獻:
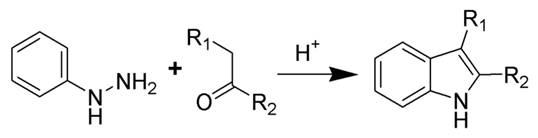
這是一個可從苯肼和一個醛或是酮類於酸性環境下產生芳香雜環吲哚。該反應是費雪於1883年所發現,目前用於治療偏頭痛的藥物中很多就是利用這個反應製備的,反應如下圖:
此反應中對於布氏酸的選擇是相當重要的,例如鹽酸、硫酸、堆磷酸及對甲苯磺酸都曾成功試驗。路易士酸的選擇如三氟化硼、氯化鋅、氯化鐵、氯化鋁等也成功應用於該反應的催化。
反應機制首先是由是醛酮與苯肼在酸催化下縮合生成苯腙,苯腙在酸催化下異構化為烯胺,並發生一個[3,3] σ遷移反應生成二亞胺。該亞胺芳構化後成環,得到一個縮醛胺。氨基質子化,離去氨,並接著失去一個質子生成芳香性的吲哚環。
Buchwald改進法:
芳基溴化物在鈀和BINAP催化下也可以與腙反應生成吲哚環,由MIT的Stephen Buchwald首先發現。
二、費雪投影式(Fischer projection)
於1891年提出,表示單糖鏈形結構、胺基酸等有機化合物結構的一種常用方法。此投影式為平面結構,所有鍵呈直向或橫向排列,碳原子編號從靠近羰基的一端開始。碳鏈縱向排列,羰基位於最上端,橫線代表鍵在紙面上,豎線代表鍵伸進紙面。
費雪投影式表現化合物的立體化學性質,可以有效地區分手性異構體。糖類的環形結構可用哈沃斯透視式(Haworth投影式)來表示。在轉化費歇爾投影式為哈沃斯透視式時,以葡萄糖為例,先將5號碳的三個基團按順時針方向旋轉至羥基處於豎直方向,然後醛基與5號碳的羥基形成半縮醛產生α-和β-兩種吡喃葡萄糖異構體,畫出平面上下的基團,再旋轉即可。
三、費雪噁唑合成(Fischer oxazole synthesis)
費雪於1896年發現,此為提供一雜環芳香噁唑合成的方式,可從氰醇和醛類於無水鹽酸中製備。
四、費雪糖苷化反應(Fischer glycosidation)
醛糖或酮糖與醇在酸催化下反應,生成糖苷。 此反應由德國化學家赫爾曼‧埃米爾‧費歇爾在1893~1895年期間發現。
一般反應是以醇為溶劑,製成糖在醇中的溶液或懸浮液。反應為一平衡,產物是多種異構體的混合物,包括環元數不同、端基異構產物以及少量鏈型糖。以己糖為原料時,反應時間較短時主要生成呋喃糖,反應時間較長時則主要產生吡喃糖。長時間反應也會使產物轉變為熱力學上更為穩定的α-端基異構體。
五、費雪酯化反應,又稱Fischer–Speier酯化反應(Fischer esterification)
此為費雪最為重要的反應,利用羧酸與醇在酸催化下迴流反應,產生酯類。常用催化劑為硫酸、對甲苯磺酸等質子酸或三氟甲磺酸鈧等路易斯酸。反應一般不加
入其它溶劑,有時也在非極性溶劑(如甲苯)進行。反應時間約為1~10小時,溫度60~110°C。
參考資料:
1. http://zh.wikipedia.org/zh-tw/%E … A%E5%90%88%E6%88%90
2. http://zh.wikipedia.org/zh-tw/%E … 5%E5%BD%B1%E5%BC%8F







 前一篇文章
前一篇文章 下一篇文章
下一篇文章 【2019 年諾貝爾生理或醫學獎】一窺細胞如何「氧」尊處優
【2019 年諾貝爾生理或醫學獎】一窺細胞如何「氧」尊處優  海芭夏 (Hypatia of Alexandria)
海芭夏 (Hypatia of Alexandria)  【2011諾貝爾化學獎】具有黃金比例的晶體
【2011諾貝爾化學獎】具有黃金比例的晶體  【2014諾貝爾化學獎】如何將光學顯微鏡變成奈米顯微鏡
【2014諾貝爾化學獎】如何將光學顯微鏡變成奈米顯微鏡  化學傳記:法拉第不為人知的一面(六):電磁轉動與電磁感應
化學傳記:法拉第不為人知的一面(六):電磁轉動與電磁感應 ![[講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講](https://highscope.ch.ntu.edu.tw/wordpress/wp-content/uploads/2015/10/Aaron-Ciechanover222.png) [講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講
[講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講  【丁肇中獲頒諾貝爾物理獎40週年專題】1976年諾貝爾物理獎官方新聞稿
【丁肇中獲頒諾貝爾物理獎40週年專題】1976年諾貝爾物理獎官方新聞稿  化學的填字遊戲?
化學的填字遊戲? 
