氯化物(Chloride)
氯化物(Chloride)
國立新莊高級中學陳偉民退休教師
當氯元素(一種鹵素)原子得到一個電子,形成陰離子(帶負電的離子)時,就形成氯離子Cl−。氫氯酸形成的鹽含有氯離子,因此也可以稱為氯化物。氯離子及其形成的鹽類,如氯化鈉,通常極易溶於水。我們全身的體液中都含有氯離子,其對傳遞神經脈衝,及調節液體進出細胞等功能非常重要。也有些含氯離子的鹽類難溶於水,如氯化銀。
氯化物中不一定含有氯離子,有些化合物中含有一個或多個以共價鍵鍵結的氯原子。例如氯化甲烷(CH3Cl)就是有機共價化合物,其中不含氯離子。
鏽蝕
含氯化物之物質,如海水,會經由自催反應,加速金屬孔洞的形成與擴大,明顯加劇大多數金屬(包含不鏽鋼及其他合金)的孔蝕(pitting corrosion)現象。整個過程簡述如下:
陽極區之半反應:Fe → Fe2+ +2e–
陰極區之半反應:1/2 O2 + H2O + 2e– → 2OH–
陽極區因鏽蝕而出現孔洞,孔洞中金屬陽離子多,使外界氯離子進入坑洞,金屬氯化物再與水反應,造成孔洞內酸性升高。
FeCl2 + 2H2O → Fe(OH)2 + 2HCl
酸性會耗去陰極區的氫氧離子,更加速鏽蝕的速率。
用途
氯化物可以製造保存食物的鹽類,如氯化鈉。氯化鈉是氯化物的一種,化學式為 NaCl。在水中,可以解離成 Na+ 與 Cl− 兩種離子。其餘含氯鹽類如氯化鈣、氯化鎂、氯化鉀有各種不同用途,包括醫療及形成水泥等。
氯化鎂,MgCl2,使用於醫藥中,作為鎂離子的來源,鎂離子在許多細胞活動中佔有重要角色,也可以作為瀉藥。
氯離子也在澱粉酶(amylase)中作為輔基(prosthetic group)。澱粉酶可催化麥芽糖(maltose)分子的分解反應。只有在氯離子存在時,這種酵素才能正常工作。沒有氯離子,澱粉酶就無法催化反應。
氯化鈣的化學式為CaCl2,在市面上,氯化鈣被製成顆粒狀的鹽,作為房間的除濕劑。因為氯化鈣可加速混凝土凝固,在建築工地,氯化鈣被用來強化路基,但如前所述,氯化物會加速金屬鏽蝕,所以應避免添加於鋼骨結構之工地。又因為氯化鈣被加到冰上時,可有效降低冰的熔點,所以在寒帶國家被廣泛被用為除冰劑。
在石油工業的開採過程中,會嚴密檢視泥土中的氯化物含量。泥土裡的氯化物若增加,可能顯示快要挖到高壓海水。氯化物升高也顯示開採目標的品質不佳。
對汙水或飲用水而言,氯化物是活性小的溶質,且無所不在,因此氯化物也是有用且可信賴的化學指標,可顯示河流/地下水是否受到排泄物汙染。世界各地的水處理公司都使用氯化物檢驗河流及飲用水源的汙染程度。
以共價鍵形成的無機氯化物有幾下數種例子,經常在化學實驗室或化工廠中作為反應試劑:
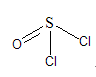
●三氯化磷、五氯化磷、亞硫醯氯(Thionyl chloride,如圖1),這三種都是實驗室裡常用的活性氯化劑。
●二氯化二硫(S2Cl2)可使橡膠硫化。
氯化汞(HgCl2)是毒性很強的化合物,由於Hg的電負度是2.0,Cl的電負度是3.16,二者電負度相差不大,形成的化合物,不算鹽類,而是分子。氯化汞的熔點為276℃,沸點為304℃,在室溫時略有揮發性,在100℃時會大量揮發。氯化汞會破壞黏膜,可作為抗菌劑及消毒劑,曾經被用來治療梅毒,但因具有毒性,現在已經不被使用醫藥。
人體健康
氯化物是人體新陳代謝(把食物變成能量的過程)必須的化學物質,血液中氯化物的量由腎臟密切控制。
.
參考資料:
1. 氯化物 http://en.wikipedia.org/wiki/Chloride
2. http://www.gopetsamerica.com/substance/chlorides.aspx
3. 氯化汞 http://en.wikipedia.org/wiki/Mercury(II)_chloride
4. http://www.substech.com/dokuwiki/doku.php?id=pitting_corrosion
5. http://www.concreteconstruction.net/concrete-construction/using-calcium-chloride-for-industrial-floor-const.aspx


 前一篇文章
前一篇文章 下一篇文章
下一篇文章 暖暖包的原理
暖暖包的原理  化學傳記:法拉第不為人知的一面(一):時至今日為何重提法拉第?
化學傳記:法拉第不為人知的一面(一):時至今日為何重提法拉第?  【2014諾貝爾化學獎】如何將光學顯微鏡變成奈米顯微鏡
【2014諾貝爾化學獎】如何將光學顯微鏡變成奈米顯微鏡  【2019諾貝爾化學獎】鋰離子電池
【2019諾貝爾化學獎】鋰離子電池  莫耳和公斤單位的重新定義
莫耳和公斤單位的重新定義 
