鹼金屬和鹼土金屬
鹼金屬和鹼土金屬 (Alkali Metals and Alkaline Earth Metals)
高雄市立女子高級中學化學科洪瑞和老師/國立中山大學化學系張祖辛副教授責任編輯
鹼金屬元素的價層電子結構為ns1。由於每一個週期都是從鹼金屬元素開始的,因此鹼金屬元素的原子都比前一週期元素的原子多了一個電子層,它們的原子半徑在同一週期中都是最大的。鹼金屬原子的次外層具有惰性氣體原子的穩定電子層結構,對核電荷的遮蔽效應較大,所以它們的第一游離能在同一週期中是最小的。
鹼金屬原子很容易失去一個電子而呈+1氧化數,低游離能和低電負度使鹼金屬元素的金屬性很強。從鹼金屬元素具有很大的第二游離能來看,它們不會失去第二個電子,因此不會表現出其他氧化數。
鹼金屬元素和鹼土金屬元素在與非金屬元素化合時,雖然多以形成離子鍵為主,但在某些情況下仍呈現出一定程度的共價性。鋰和鈹元素由於原子半徑小,游離能較其他同族元素高,所以形成共價鍵的傾向比較顯著(少數鎂的化合物也是共價性較強);常常表現出與同族其他元素不同的化學性質。在同一族中,鹼金屬元素和鹼土金屬元素從上至下,原子半徑依次增大,游離能和電負度依次減小,金屬活潑性依次增強。
鹼金屬元素和鹼土金屬元素的金屬性很強,只能以化合物的形式存在於自然界中。鈣、鈉、鉀和鎂元素在地殼中的豐度均很高,而鋰、鈹、銣、銫含量很低屬於稀有金屬,鍅和鐳則為放射性元素。
鹼金屬和鹼土金屬都具有金屬光澤,有良好的導電性和延展性。除了鈹和鎂單質以外,其他鹼金屬和鹼土金屬都很軟,可以用刀子切割。金屬鋰、鈉和鉀的密度小於1g /cm3,比水的密度小,會浮在水面上。鹼金屬元素的原子只有一個價電子,且原子半徑較大,故形成的金屬鍵很弱,因此,鹼金屬單質的熔點、沸點較低。其中銫的熔點最低,只有28. 44℃,是熔點略高於汞的低熔點金屬。
金屬銫中的自由電子活性極大,當其表面受到光照時,電子便獲得能量從表面逸出,利用這種特性,銫被用來製作光電管中的陰極。鹼土金屬元素的原子有2個價電子,與同周期的鹼金族相比,金屬鍵較強,因此鹼土族金屬的熔點、沸點、密度和硬度都比鹼金族高。
化學性質方面,鹼金屬和鹼土金屬都是很活潑的金屬,它們都能與大多數非金屬反應。如它們極易在空氣中燃燒。在鹼金屬和鹼土金屬中,除金屬鈹和鎂由於表面形成一層緻密的保護膜對水穩定外,其他金屬單質都容易與水發生反應形成穩定的氫氧化物,這些氫氧化物大多是強鹼,例如:NaOH、Ca(OH)2。這些反應放出大量的熱,因此金屬鈉與水發生劇烈作用;金屬鉀、銣、銫遇水則會燃燒甚至發生爆炸。金屬鋰、鈣、鍶和鋇與水反應比較緩慢,其原因是這幾種金屬的熔點較高,反應中放出的熱,不足以使它們熔化成液體;另外這幾種金屬元素的氫氧化物的溶解度較小,它們覆蓋在金屬固體表面,使金屬與水的反應速率降低。
鹼金屬元素和鹼土金屬元素化合物在高溫火焰中,可以發出特定的顏色,這種現象稱為焰色反應。金屬原子的外圍電子受高溫火焰的激發而躍遷到較高能階軌域上,當電子從高能階返回到低能階時,就會發射出特定波長(頻率)的光束,使火焰呈現出它們的特徵焰色:鋰為深紅色;鈉為黃色、鉀為紫色、銣為紫紅色、銫為藍色、鈣為磚紅色、鍶為紅色、鋇為綠色。
鹼金屬元素和鹼土金屬化合物大多數是離子型化合物。它們的離子易和水分子結合成穩定的水合離子:M+(aq)和M2+(aq)而且都是無色的。鹼金屬離子與同週期的鹼土金屬離子相比,有較大的離子半徑和較小的電荷,同時它們的離子最外電子層結構符合八隅體(Li+、Be2+除外)。所以鹼金屬的氫氧化物和鹽,大多易溶於水,氫氧化物和鹽的溶解度比鹼土金屬更大。
鹼金屬在空氣中燃燒時,金屬鋰主要生成LiO,而金屬鈉、鉀、銣和銫主要生成Na2O2、KO2、RbO2和CsO2。鹼金屬氧化物和鹼土金屬氧化物的熱穩定性的大趨勢是從Li2O到Cs2O、從BeO到BaO逐漸降低。鹼金屬氫氧化物和鹼土金屬氫氧化物都是白色晶體,在空氣中易吸水潮解,所以NaOH和Ca(OH)2晶體 皆可作為乾燥劑。鹼金屬氫氧化物易溶於水,而鹼土金屬氫氧化物在水中的溶解度較小。鹼金屬氫氧化物的溶解度從LiOH到CsOH依次增大;鹼土金屬氫氧化物的溶解度從Be (OH)2到Ba(OH)2也依次遞增,而Be(OH)2和Mg(OH)2則難溶於水。
參考資料:
1. Geoff Rayner-Canham, Tina Overton, 2006, Descriptive Inorganic Chemistry, 4th ed., Freeman.
2. 司學芝、劉捷、展海軍,2009年,無機化學,化學工業出版社。


 前一篇文章
前一篇文章 下一篇文章
下一篇文章 【2019諾貝爾化學獎】鋰離子電池
【2019諾貝爾化學獎】鋰離子電池  化學傳記:法拉第不為人知的一面(九):法拉第和社會的關係
化學傳記:法拉第不為人知的一面(九):法拉第和社會的關係  謎樣的分子:克里奇中間體
謎樣的分子:克里奇中間體 ![[講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講](https://highscope.ch.ntu.edu.tw/wordpress/wp-content/uploads/2015/10/Aaron-Ciechanover222.png) [講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講
[講座] Aaron Ciechanover 教授(2004諾貝爾化學獎得主)醫藥通俗演講  化學的填字遊戲?
化學的填字遊戲? 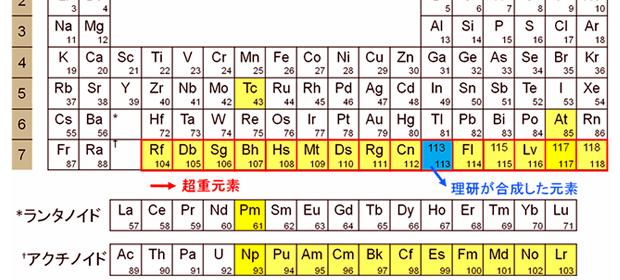 原子序第113超重元素的發現與命名
原子序第113超重元素的發現與命名  【2014諾貝爾化學獎】如何將光學顯微鏡變成奈米顯微鏡
【2014諾貝爾化學獎】如何將光學顯微鏡變成奈米顯微鏡 

請問最後一段的LiO, KO2, RbO2是這樣嗎?