含氧雜環(上)
含氧雜環(上)(Oxygen Heterocyclic Ring (I))
國立臺灣師範大學化學系碩士生 鍾長志
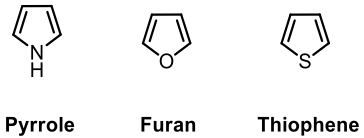
在有機化學領域中,雜環化合物 (heterocyclic compound, heterocycle),1扮演重要的角色。根據 IUPAC 的定義,雜環化合物為「在環形分子中,具有至少兩種不同的元素之環狀化合物」。而常見的有機雜環分子中,以含氧雜環、含氮雜環,含硫雜環最為常見,如圖一所示,而本篇將著重於介紹含氧三員~七員雜環及常見的製備方式。
含氧雜環種類眾多,可以先以形成之環數簡單分類,再以下列方式細分:1
- 飽和 (saturation) 及不飽和 (unsaturated) 環形化合物
- 含氧之環形化合物
- 同時含氧及其他雜原子的環形化合物
- 位置異構物 (positional isomer) 環形化合物
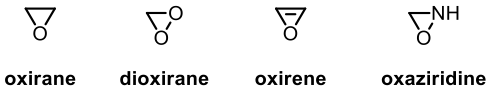
A. 含氧三員環,常見結構及俗名如圖二所示
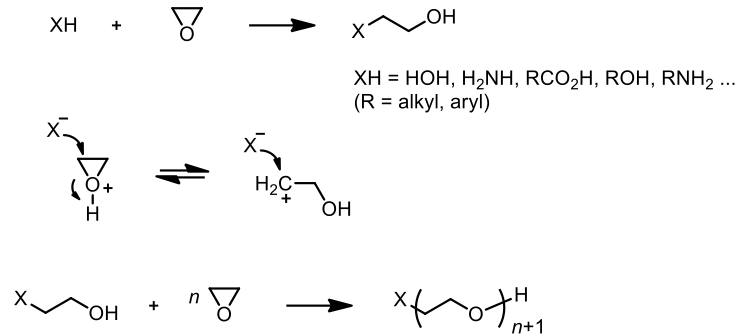
環氧乙烷 (ethylene oxide, or oxirane),為一種的環狀醚類化合物 (cyclic ethers),因三員環的關係使之容易開環 (decyclization),具有非常好的反應性,應用於非常多的加成反應 (addition reaction) 和聚合反應 (polymerization)(圖三)。2
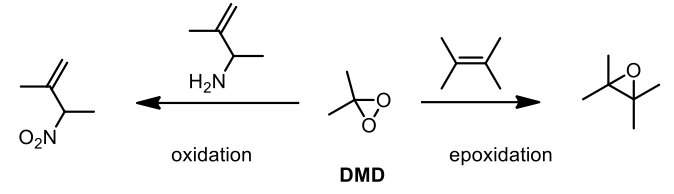
二氧環丙烷 (dioxirane),又稱雙環氧乙烷,是一個不穩定的化合物,在有機合成中,此類化合物最常見的是 3,3-雙甲基二氧環丙烷 (3,3-dimethyldioxirane, DMD),因其不穩定性質,容易進行反應,被廣泛應用於氧化反應 (oxidation reaction) 以及環氧化 (epoxidation),如圖四所示。3
氧環丙烯 (oxirene),又稱氧吮,目前無法確定是否真實存在,不過有文獻提出它可能存在於反應之中為中間體。
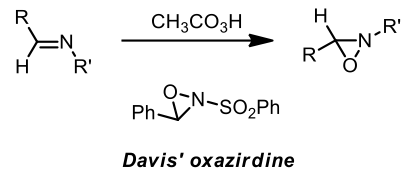
氧氮環丙烷 (oxaziridine),因三員環以及氮氧鍵較弱的關係,使之容易開環進行反應。在西元 1956 年,被 William D. Emmons 合成,1970 年代,Franklin Davis 合成出以它為名的 Davis’ oxazirdine,其被廣泛應用有機合成以及不對稱合成中(圖五)。4
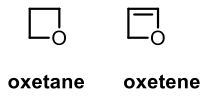
B. 含氧四員環,常見結構及俗名如圖六所示
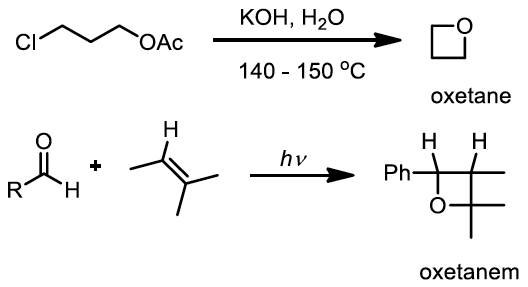
氧環丁烷 (oxetane),又稱氧呾,於 1949 年 Noller 實驗室,以氫氧化鉀 (potassium hydroxide, KOH) 及加熱的條件下製備氧環丁烷;與 1954 年由 Büchi 實驗室,以照光的方式合成出 oxetanem (圖七)。5,6,7
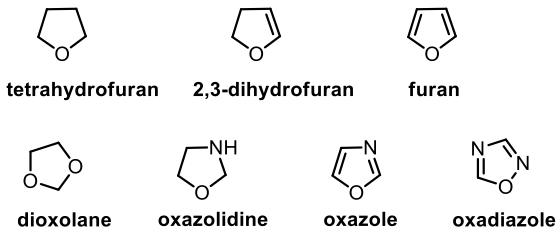
C. 含氧五員環,常見結構及俗名如圖八所示
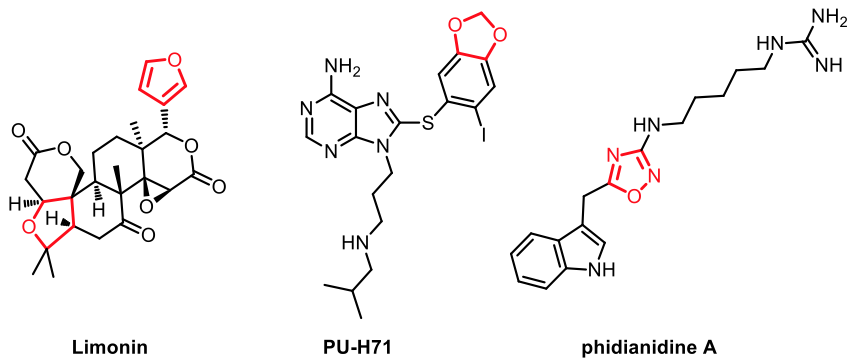
五員環中的含氧雜環種類繁多。在常見的五員環雜環中同時具有氧以及氮之雜原子的也有非常多種。在天然物結構中,可以容易找到含氧原子之五員環(圖九)。
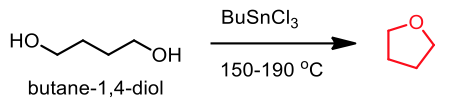
含氧五員環結構的化合物之合成方式有非常多,下面僅列舉少數。下圖為四氫呋喃 (tetrahydrofurane) 的合成,利用路易士酸以及加熱的條件下將 1,4-丁二醇 (butane-1,4-diol) 進行分子內環化得到,如圖十。8
下圖十一為含二氫呋喃 (dihydrofuran) 結構之化合物,可以透過硝基羥醛縮合反應 (nitro-aldol reaction) 合成得到。9
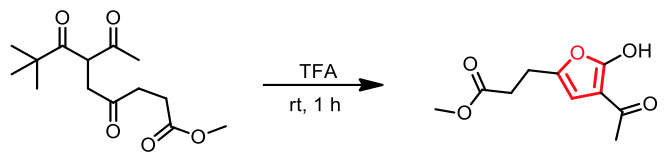
具呋喃 (furane) 結構之化合物的合成,透過巴爾-諾爾合成 (Paal-Knorr synthesis) 的方法可以得到呋喃類似物(圖十二)。10
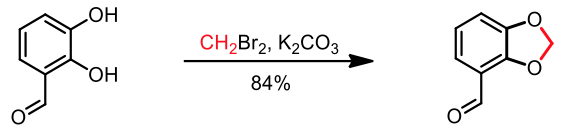
具二草酸酯 (dioxolane) 結構之化合物的合成,可透過二溴乙烷以及碳酸鉀的條件下進行親核反應得到(圖十三)。11
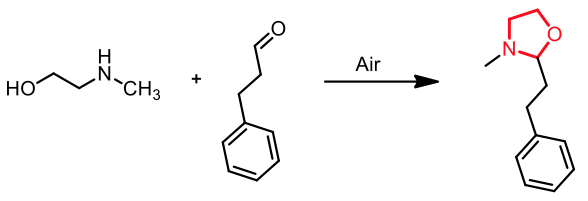
(口咢)唑啶 (oxazolidine) 結構之化合物的合成,透過空氣的條件下進行反應,進行親核反應可以得到(圖十四)。12
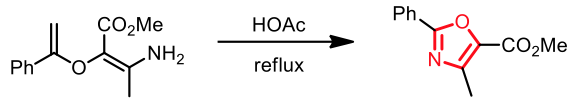
噁唑 (oxazole) 結構之化合物的合成,透過 Robinson — Gabriel synthesis 的概念進行分子內環化反應,可以得到噁唑化合物(圖十五) 。13
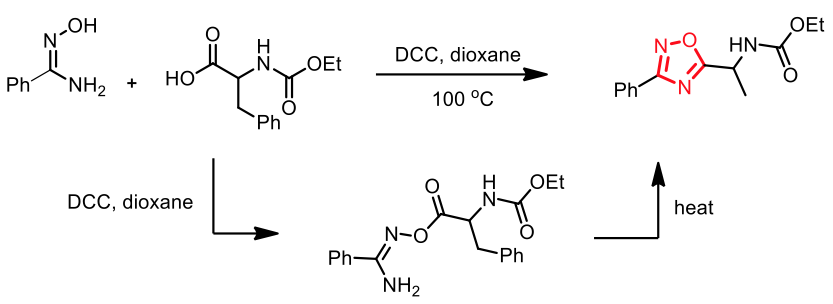
(口咢)二唑 (oxadiazole) 結構之化合物的合成,利用 N,N‘-二環己基碳二亞胺 (N,N‘-Dicyclohexylcarbodiimide, DCC) 以及加熱的條件下進行環化反應,如圖十六所示。14
連結:含氧雜環(下)
參考文獻
- Alvarez‐Builla, J., & Barluenga, J. (2012). Heterocyclic Compounds: An Introduction. ChemInform, 43(1), no.1–9.
- Rebsdat, S., & Mayer, D. (2001). Ethylene oxide. Ullmann’s Encyclopedia of industrial chemistry. 547–72.
- Overman, L. E. (2002). Organic Reactions. Vol 61.
- Emmons, W. D. (1956). The synthesis of oxaziranes. Journal of the American Chemical Society, 78(23), 6208-6209.
- Büchi, G., Inman, C. G., & Lipinsky, E. S. (1954). Light-catalyzed organic reactions. I. The reaction of carbonyl compounds with 2-methyl-2-butene in the presence of ultraviolet light. Journal of the American Chemical Society, 76(17), 4327-4331.
- D’Auria, M., & Racioppi, R. (2013). Oxetane synthesis through the Paternò-Büchi reaction. Molecules, 18(9), 11384-11428.
- Noller, C. R. (1949). TRIMETHYLENE OXIDE-OXETANE. ORGANIC SYNTHESES, 29, 92-93.
- Tagliavini, G., Marton, D., & Furlani, D. (1989). Organotins as etherfication catalysts. 11. catalytic conversion of alcohols to open-chain and cyclic ethers by organotin trichlorides. Tetrahedron, 45(4), 1187-1196.
- Amantini, D., Fringuelli, F., Piermatti, O., Pizzo, F., & Vaccaro, L. (2003). 3-Nitrocoumarins as dienophiles in the Diels-Alder reaction in water. An approach to the synthesis of nitrotetrahydrobenzo [c] chromenones and dihydrodibenzo [b, d] furans. The Journal of organic chemistry, 68(24), 9263-9268.
- Stauffer, F., & Neier, R. (2000). Synthesis of tri-and tetrasubstituted furans catalyzed by trifluoroacetic acid. Organic letters, 2(23), 3535-3537.
- Rigby, J. H., Maharoof, U. S., & Mateo, M. E. (2000). Studies on the narciclasine alkaloids: total synthesis of (+)-narciclasine and (+)-pancratistatin. Journal of the American Chemical Society, 122(28), 6624-6628.
- Al-Masum, M., Lott, B. W., & Ghazialsharif, N. (2012). An efficient reaction process for the synthesis of oxazinanes, and oxazolidines in the presence of air.
- Liu, X., Cheng, R., Zhao, F., Zhang-Negrerie, D., Du, Y., & Zhao, K. (2012). Direct β-acyloxylation of enamines via PhIO-mediated intermolecular oxidative C–O bond formation and its application to the synthesis of oxazoles. Organic letters, 14(21), 5480-5483.
- Braga, A. L., Lüdtke, D. S., ALBERTA, E. E., Dornelles, L., SEVERO, W. A., Corbellini, V. A., … & Schwab, R. S. (2004). ‘One-pot’synthesis of chiral N-protected α-amino acid-derived 1, 2, 4-oxadiazoles. Synthesis, (10), 1589-1594.


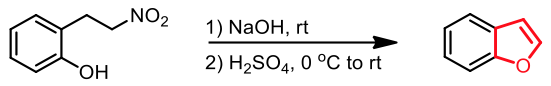
 前一篇文章
前一篇文章 下一篇文章
下一篇文章 化學傳記:法拉第不為人知的一面(十一):凡人法拉第
化學傳記:法拉第不為人知的一面(十一):凡人法拉第  【2014諾貝爾化學獎】如何將光學顯微鏡變成奈米顯微鏡
【2014諾貝爾化學獎】如何將光學顯微鏡變成奈米顯微鏡  油理油趣─淺談食油的化學
油理油趣─淺談食油的化學  暖暖包的原理
暖暖包的原理 ![[講義] 科學史沙龍:陳竹亭教授、楊信男教授](https://highscope.ch.ntu.edu.tw/wordpress/wp-content/uploads/2015/01/科學史.png) [講義] 科學史沙龍:陳竹亭教授、楊信男教授
[講義] 科學史沙龍:陳竹亭教授、楊信男教授  目前世界上最精準的時鐘-光晶格光頻原子鐘在低溫環境下的突破
目前世界上最精準的時鐘-光晶格光頻原子鐘在低溫環境下的突破  【2015諾貝爾化學獎特別報導】DNA修補─為生命提供化學的穩定
【2015諾貝爾化學獎特別報導】DNA修補─為生命提供化學的穩定 
