克服胰島移植急性排斥的新希望
克服胰島移植急性排斥的新希望
國立臺灣大學生命科學系助教范姜文榮

糖尿病重症患者必須終其一生都持續不斷地注射胰島素。如果要找到將糖尿病重症患者從注射胰島素中解放的終極治療法,必須將製造胰島素的胰島細胞移植到糖尿病患的肝臟內,且確保細胞能永遠存活,才能根治糖尿病。(圖片來源:flickr用戶 sarihuella)
資料來源:福岡大學新聞稿2013年6月4日
糖尿病重症患者必須終其一生持續不斷地注射胰島素。如果要將患者從終生注射胰島素中解放,必須將正常製造胰島素的胰島細胞移植到糖尿病患的肝臟內且能永遠存活,才能根治糖尿病。全世界從2000年到2012年為止約已進行約700例的胰島細胞移植手術,但是胰島細胞提供者的數量有限,造成胰島細胞供應嚴重不足。即便使用免疫抑制劑,胰島細胞移植數小時後就會引發早期免疫排斥反應,造成細胞被破壞。因此往往要從2~3個人取下的胰島細胞,才能滿足單一患者達到治療效果的需求。因此如何防止胰島細胞移植引發的早期免疫排斥反應,成為移植醫學一個亟待克服的問題。
先前研究發現胰島細胞移植後短時間就會引發早期排斥反應,確認是因自胰島細胞釋放出的HMGB1核內蛋白質所引起。HMGB1蛋白質會活化免疫系統的NKT細胞及多核形白血球,進而引發早期排斥反應。但是被移植的胰島細胞究竟透過何種機制將HMGB1蛋白質釋放至細胞外,仍未被了解。故認為瞭解其機制,有助開發出抑制早期排斥反應、效果較佳的控制法。
日本研究團隊發現移植到肝臟門靜脈的胰島細胞會立即暴露於低氧狀態,活化胰島細胞膜上的Na+/Ca2+交換輸送體 (Sodium-Calcium Exchanger),使得大量鈣離子流入細胞,導致胰島細胞死亡,而將HMGB1蛋白質釋放到細胞外。為了避免胰島細胞在移植死亡,研究團隊想到在移植胰島細胞前如果先用Na+/Ca2+交換輸送體的抑制劑處理細胞,使鈣離子不會流入胰島細胞,是否就可以防止細胞死亡與HMGB1蛋白質釋放所引起的免疫排斥?利用小鼠作實驗,結果發現Na+/Ca2+交換輸送體的抑制劑果真可以避免胰島移植所引發早期的排斥反應。 同樣的處理也可以防止人類胰島細胞因暴露於低氧狀態引發的細胞死亡。這個發現對未來延長移植胰島細胞的存活將有很大的助益。
專有名詞
胰島:以細胞團塊分佈於胰臟中,具有能生產胰島素的β細胞。β細胞會因血糖值上升而分泌胰島素到血液中。
HMGB1: high mobility group box1蛋白質的簡稱,通常存在於細胞核內,與染色質結構、遺傳密碼轉錄的調控有關。
延伸閱讀:


 前一篇文章
前一篇文章 下一篇文章
下一篇文章 2014諾貝爾化學獎的遺珠:結構光照明顯微法
2014諾貝爾化學獎的遺珠:結構光照明顯微法 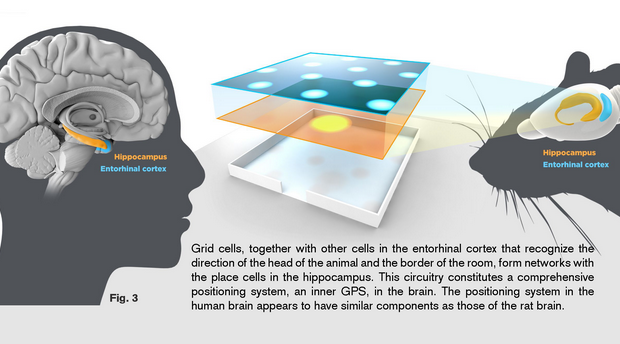 【2014諾貝爾生醫獎】發現大腦裡空間記憶的構築細胞
【2014諾貝爾生醫獎】發現大腦裡空間記憶的構築細胞  國際生物多樣性日專題 – 何謂生物多樣性?
國際生物多樣性日專題 – 何謂生物多樣性?  使用 CRISPR 技術清除體內的愛滋病病毒
使用 CRISPR 技術清除體內的愛滋病病毒  偵測到大爆炸微波輻射的研究持續受到質疑
偵測到大爆炸微波輻射的研究持續受到質疑 ![[影音] CASE【百秒說科學】什麼是魅夸克?](https://highscope.ch.ntu.edu.tw/wordpress/wp-content/uploads/2016/07/J粒子-科學online.png) [影音] CASE【百秒說科學】什麼是魅夸克?
[影音] CASE【百秒說科學】什麼是魅夸克?  伊波拉病毒(II)-「無知與不信任」才是真正的敵人
伊波拉病毒(II)-「無知與不信任」才是真正的敵人  玄奧難明的水
玄奧難明的水 
