似氫原子2s軌域的解析(上)
似氫原子2s軌域的解析(上) Analytical 2s orbital of hydrogen like atom (I)
國立臺灣師範大學化學系兼任教授 邱智宏教授
高中化學教授原子軌域及混成軌域時,總會有好奇的學生抛出似懂非懂的問題:$$1s$$ 和 $$2s$$ 軌域均為圓球的形狀,它們除了大小不同以外,其他都一樣嗎?電子隨徑向(radial)呈現不均勻的分佈,也只會出現一個最可能半徑(the most probable radius)嗎?
常聽老師說在軌域中電子不會出現的地方稱有節點、節面(nodel plane)和節球面(nodel surface),$$2s$$ 軌域含有一個節球面,則電子在內層球體中出現的機率究竟為多少?另外,論及 $$2s$$ 和 $$2p$$ 的混成軌域時,總將 $$2s$$ 的波函數圖形,以 $$1s$$ 軌域來類比,這樣的假設是否合理?本文擬以似氫原子的 $$2s$$ 軌域為例,試圖解答學生的上述問題。
一、似氫原子的$$2s$$波函數及其特性
由薛丁格方程式(Schrödinger equation)解出的似氫原子(hydrohen like atom) $$1s$$、$$2s$$ 波函數分別如下:
$$\displaystyle\varphi_{1s}=\frac{1}{\sqrt{\pi}}(\frac{Z}{a_0})^{3/2}e^{-Zr/a_0}$$
$$\displaystyle\varphi_{2s}=\frac{1}{4\sqrt{2\pi}}(\frac{Z}{a_0})^{3/2}\left(2-\frac{Zr}{a_0}\right)e^{-Zr/2a_0}$$
其中 $$a_0$$ 為波耳半徑等於 $$0.53\overset{\circ}{A}$$,$$Z$$ 為原子核的正電數,對於氫原子而言 $$Z=1$$。氫原子唯一的一個電子若填在能階最低的 $$1s$$ 軌域上稱為基態(ground state),若填在 $$2s$$ 軌域上則為激態(excited state)。
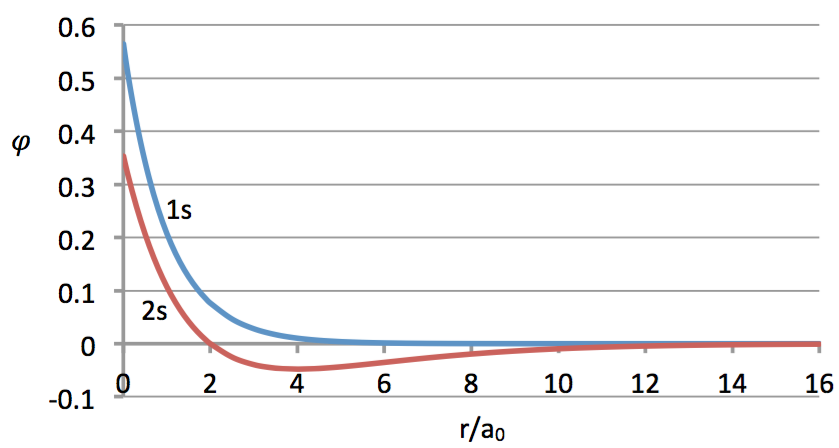
將其波函數對半徑作圖可得圖一,其中 $$x$$ 座標的刻度為 $$r/a_0$$,由圖中可看出 $$1s$$ 波函數在 $$r=0$$ 最大,隨著 $$r$$ 值的增大遞減的很快,而 $$2s$$ 波函數雖然也是在 $$r=0$$ 最大,但在某一個特殊的位置其波函數為零,代表此處電子出現的機率為 $$0$$,由上列 $$2s$$ 的波函數可知,在 $$r$$ 不是無限大時,指數部分不可能為 $$0$$,因此唯有 $$\left(2-\frac{Zr}{a_0}\right)=0$$ 時,波函數才有可能為 $$0$$,因此 $$r=\frac{2a_0}{Z}$$ 時即為節球面出現的位置。
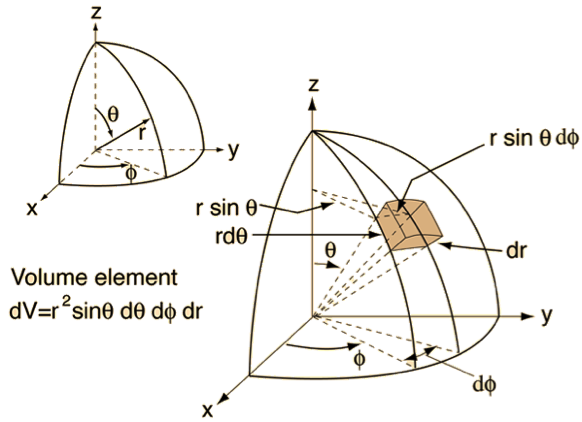
如果要探究距離原子核從 $$r$$ 到 $$r+dr$$,$$\theta$$ 到 $$\theta+d\theta$$,$$\phi$$ 到 $$\phi+d\phi$$ 之間的單位體積內找到電子的機率有多大?則必需計算其間體積的變化量再乘上該處的電子機率密度($$|\varphi|^2$$)。由圖二可看出極座標單位體積($$dV$$)的變化量為:
$$dV=r\sin\theta d\phi\times rd\theta\times dr=r^2\sin\theta~d\theta~d\phi~dr$$
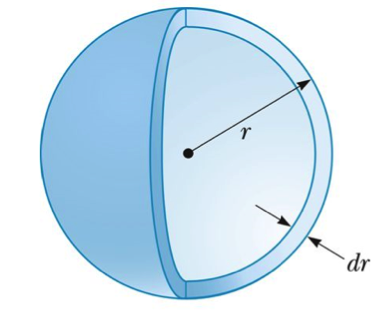
由於 $$1s$$ 和 $$2s$$ 軌域和 $$\theta$$、$$\phi$$ 無關,因此可單看徑度變化的影響如圖三所示,探索在從 $$r$$ 到 $$r+dr$$ 間圓殼(spherical shell)內找到電子的機率有多少?
若將 $$dV$$ 乘上機率密度並將 $$\theta$$、$$\phi$$ 積分,即能檢驗徑度變化對電子出現機率的影響:
$$\begin{array}{ll}\displaystyle \left|\varphi\right|^2r^2dr\int^{2\pi}_{0}d\phi\int^{\pi}_{0}\sin\theta ~d\theta&=|\varphi|^2r^2dr\times(2\pi-0)\times(-\cos\pi+\cos 0)\\&=|\varphi|^2r^2dr\times(2\pi)\times 2=4\pi|\varphi|^2r^2dr\end{array}$$
若將上式的 $$4\pi|\varphi|^2r^2$$ 對 $$r$$ 作圖可得圖四,其中 $$x$$ 座標的刻度為 $$r/a_0$$。由圖中可看出氫原子 $$1s$$ 和 $$2s$$ 軌域在徑向的機率密度分佈情形。其中 $$1s$$ 軌域除了在 $$r=0$$ 及 $$r=\infty$$ 時電子出現的機率密度為 $$0$$ 以外,並没有出現節球面的情形,而 $$2s$$ 則在 $$r=2a_0/Z$$ 時出現一個節球面,和上述計算的結果相符,因為 $$Z=1$$,所以 $$r=2a_0$$,若 $$Z$$ 不等於 $$1$$ 的似氫原子時,節球面會出現在更靠近原子核的地方。
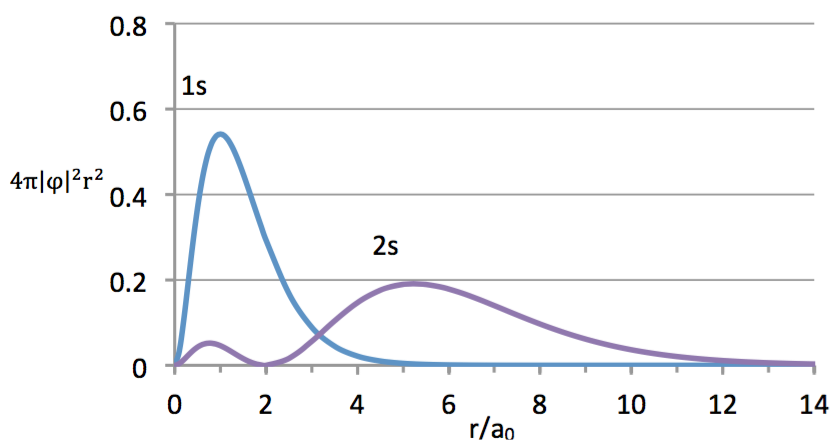
圖四 氫原子 $$1s$$ 和 $$2s$$ 軌域的徑向函數 $$(4\pi|\varphi|^2r^2)$$ 對 $$r/a_0$$ 作圖,由其徑向電子的機率分佈情形可看出 $$2s$$ 有二個極大值,節球面出現在 $$r=2a_0$$ 的位置。(來源:作者繪製)
由圖中亦可看出 $$2s$$ 的電子機分佈圖有二個極大值,可經由微分下式並令其為 $$0$$ 求出:
$$\displaystyle\frac{\partial 4\pi|\varphi_{2s}|^2r^2}{\partial r}=\displaystyle\frac{\partial\left[\frac{1}{8}(\frac{Z}{a_0})^3\left(2-\frac{Zr}{a_0}\right)^2r^2e^{-Zr/a_0}\right]}{\partial r}$$
$$=\displaystyle\frac{1}{8}(\frac{Z}{a_0})^3\left[2\times\left(2-\frac{Zr}{a_0}\right)\left(\frac{-Z}{a_0}\right)r^2e^{-\frac{Zr}{a_0}}+\left(2-\frac{Zr}{a_0}\right)^22re^{-\frac{Zr}{a_0}}+\left(2-\frac{Zr}{a_0}\right)^2r^2e^{-Zr/a_0}\left(\frac{-Z}{a_0}\right)\right]$$
$$=\displaystyle\frac{1}{8}(\frac{Z}{a_0})^3\left(2-\frac{Zr}{a_0}\right)re^{-\frac{Zr}{a_0}}\left[2\times\left(\frac{-Z}{a_0}\right)r+2\times\left(2-\frac{Zr}{a_0}\right)+\left(2-\frac{Zr}{a_0}\right)r\left(\frac{-Z}{a_0}\right)\right]$$
$$=\displaystyle\frac{1}{8}(\frac{Z}{a_0})^3\left(2-\frac{Zr}{a_0}\right)re^{-\frac{Zr}{a_0}}\left[\left(\frac{Zr}{a_0}\right)^2+\left(\frac{-6Zr}{a_0}\right)+4\right]$$
電子密度函數的極小值出現在 $$r=0$$、$$r=2a_0/Z$$ 及 $$r=\infty$$ 的位置,而極大值可由上式中弧號的值等於 $$0$$ 而求出,分別為 $$r=(3-\sqrt{5})a_0/Z$$ 及 $$r=(3+\sqrt{5})a_0/Z$$,對於氫原子 $$Z=1$$,則 $$2s$$ 有二個最可能半徑,而非如 $$1s$$ 的一個,其值分別為 $$0.72$$ 及 $$5.24a_0$$,可以對照圖四中極大值出現的位置。
經計算,電子出現的機率在第二個最可能半徑為 $$0.19$$,約為第一個最可能半徑 $$0.052$$ 的 $$4$$ 倍,由圖四中二者的高度比便可以了解。接著我們想要知道若氫原子的電子填在 $$2s$$ 軌域時,則電子在第一個節球面以內的球體中出現的機率有多大?
連結: 似氫原子2s軌域的解析(下)
參考文獻
- Levine, I. N. (1988), Physical Chemistry (3rd ed.). p622~632, McGRAW-HILL Book Company.
- 葉名倉、劉如熹、邱智宏、周芳妃、陳建華、陳偉民(2013 年)高級中學化學選修上冊。南一書局。第 19~33 頁。
- Georgia State University. http://hyperphysics.phy-astr.gsu.edu/hbase/sphc.html
- Is s-p mixing referring to hybridization or is it the mixing of one atoms s orbital with the other’s p orbital? — chemistry.stackexchange.com. http://chemistry.stackexchange.com/questions/26445/is-s-p-mixing-referring-to-hybridization-or-is-it-the-mixing-of-one-atoms-s-orbi
- slide_44.jpg — CENGAGELeaning. http://images.slideplayer.com/23/6601420/slides/slide_44.jpg


 前一篇文章
前一篇文章 下一篇文章
下一篇文章 化學傳記:法拉第不為人知的一面(八):電解定律
化學傳記:法拉第不為人知的一面(八):電解定律  不需溶劑的紅血球冷凍保存方法
不需溶劑的紅血球冷凍保存方法  【2011諾貝爾化學獎】具有黃金比例的晶體
【2011諾貝爾化學獎】具有黃金比例的晶體  【2014諾貝爾化學獎深入報導】 打破光學顯微鏡的解析度極限-超高解析螢光顯微法
【2014諾貝爾化學獎深入報導】 打破光學顯微鏡的解析度極限-超高解析螢光顯微法 
